题目内容
【题目】现对三种不同的镁铝合金样品进行编号,做以下实验探究。
(1)取样品①m1g,加入过量NaOH溶液,充分反应后过滤;往滤液中通入过量CO2气体:将所得沉淀过滤、洗涤、烘干,灼烧,得到固体的质量仍然为m1g.合金中镁的质量分数为_____(保留2位小数,下同)。
(2)取样品②m2g,与足量稀硫酸反应,固体完全溶解时得到气体的体积为VL(标准状况)。m2的取值范围是_____。
(3)取样品③0.918g与30.00mL、2.00mL盐酸充分反应后,得到672mL气体(标准状况)。剩余合金0.306g(认为合金中镁、铝与酸的反应同时发生)。然后在反应后所得体系中继续加1.00mol/L的NaOH溶液,恰好使所有铝元素均不以沉淀形式存在。则需要加入1.00mol/L的NaOH溶液_____mL。
【答案】0.47 0.80V<m2<1.07V 78.00
【解析】
(1)镁铝合金样品,加入过量NaOH溶液,充分反应后过滤;往滤液中通入过量CO2气体:将所得沉淀过滤、洗涤、烘干,灼烧,得到的固体是氧化铝。
(2)镁铝合金样品,与足量稀硫酸反应,镁、铝都能与硫酸反应生成氢气,利用极值法计算m2的取值范围;
(3)镁铝合金样品,(0.918-0.306)g与30.00mL 2.00mol/L盐酸充分反应后,得到672mL气体,可计算出样品③中镁铝的含量;使所有铝元素均不以沉淀形式存在时,溶质恰好是氯化钠和偏铝酸钠。
(1)镁铝合金样品,加入过量NaOH溶液,充分反应后过滤;往滤液中通入过量CO2气体:将所得沉淀过滤、洗涤、烘干,灼烧,得到的固体是氧化铝,即Al2O3的质量与镁铝合金样品质量相等,根据元素守恒,Al2O3中氧元素的质量等于样品中Mg的质量,合金中镁的质量分数为![]() =0.47;
=0.47;
(2)生成氢气的物质的量是![]() ;假设m2g样品全是Mg,Mg+H2SO4= MgSO4+H2;则Mg的物质的量是
;假设m2g样品全是Mg,Mg+H2SO4= MgSO4+H2;则Mg的物质的量是![]() ,质量是
,质量是![]() 1.07V;假设m2g样品全是Al,2Al+3H2SO4= Al2(SO4)3+3H2;则Al的物质的量是
1.07V;假设m2g样品全是Al,2Al+3H2SO4= Al2(SO4)3+3H2;则Al的物质的量是![]() ,质量是
,质量是![]() 0.80V;所以m2的取值范围是0.80V<m2<1.07V;
0.80V;所以m2的取值范围是0.80V<m2<1.07V;
(3)设与盐酸反应的镁、铝的物质的量分别是xmol、ymol;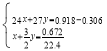 ,解得
,解得![]() ;即镁、铝的物质的量比为1:1,0.918g样品中铝的物质的量是0.018mol;使所有铝元素均不以沉淀形式存在时,溶质恰好是氯化钠和偏铝酸钠,根据氯元素守恒,氯化钠的物质的量是 0.03L× 2.00mol/L=0.06mol,根据铝元素守恒,偏铝酸钠的物质的量是0.018mol,则需要氢氧化钠的物质的量是0.018mol+0.06mol=0.078mol,需要加入1.00mol/L的NaOH溶液的体积是
;即镁、铝的物质的量比为1:1,0.918g样品中铝的物质的量是0.018mol;使所有铝元素均不以沉淀形式存在时,溶质恰好是氯化钠和偏铝酸钠,根据氯元素守恒,氯化钠的物质的量是 0.03L× 2.00mol/L=0.06mol,根据铝元素守恒,偏铝酸钠的物质的量是0.018mol,则需要氢氧化钠的物质的量是0.018mol+0.06mol=0.078mol,需要加入1.00mol/L的NaOH溶液的体积是![]() 0.078L=78.00 mL。
0.078L=78.00 mL。

【题目】金属钛(Ti)被称为21世纪金属,在航海、航空、记忆和涂料方面应用广泛,TiO2是一种优良的光催化剂。20世纪科学家尝试用多种方法将金红石(TiO2)还原,发现金红石直接氯化是冶炼钛的关键。
步骤:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g) ΔH=+1493kJmol-1,ΔS=+61JK-1mol-1
该反应发生温度高达2170℃,能耗大,对设备和生产要求几乎达到苛刻程度。目前科学家采用金红石加碳氯化方法,在较温和条件下成功制取TiCl4,为人类快速迈进钛合金时代做出了巨大贡献。金红石加碳氯化的主要反应如下:
反应Ⅰ:TiO2(s)+2Cl2(g) +C(s)![]() TiCl4(g)+CO2(g) ΔH1,ΔS1=+64JK-1mol-1
TiCl4(g)+CO2(g) ΔH1,ΔS1=+64JK-1mol-1
反应Ⅱ:TiO2(s)+2Cl2(g) +2C(s)![]() TiCl4(g)+2CO(g) ΔH2,△S2
TiCl4(g)+2CO(g) ΔH2,△S2
已知:①C(s)+O2(g)=CO2(g) ΔH=-394.3kJmol-1
②2C(s)+O2(g)=2CO(g) ΔH=-222.3kJmol-1
请回答:
(1)反应Ⅰ的ΔH1=__kJmol-1。
(2)对于气体参加的反应,表示平衡常数KP时,用气体组分B的平衡压强P(B)代替该气体物质的量浓度c(B),则反应Ⅰ的KP=__(用表达式表示)。
(3)在常温、常压、光照条件下,N2在催化剂TiO2表面与H2O发生反应,2N2(g)+6H2O(1)=4NH3(g)+3O2(g) ΔH=+1530.4kJmol-1
进一步研究相同条件下NH3生成量与温度的关系,部分实验数据见表:
实验组别 | 1 | 2 | 3 | 4 |
T/K | 303 | 313 | 323 | 353 |
NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 | 2.0 |
O2生成量/(10-6mol) | 3.6 | 4.4 | 4.5 | 1.5 |
反应时间/h | 3 | 3 | 3 | 3 |
容器体积/L | 2 | 2 | 2 | 2 |
①请在如图中画出上述反应在“有催化剂”与“无催化剂”两种情况下反应过程中体系能量随反应过程的变化趋势示意图(图中标明必要的文字说明)。___
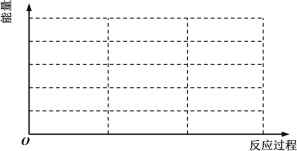
②根据表中数据,在303K时,在3h内用氮气表示其平均反应速率为___molL-1h-1。判断组别4中反应是否达到平衡状态___(填“是”或“否”),并说明理由___。