��Ŀ����
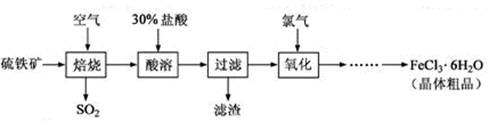
��12�֣�����������Ҫ�ɷ�ΪFeS2��Ϊԭ���Ʊ��Ȼ������壨FeCl3��6H2O���Ĺ����������£�
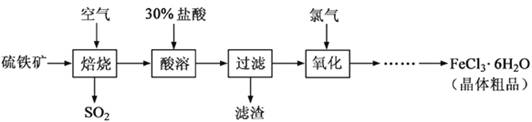
�ش��������⣺
��1����������±��յĻ�ѧ����ʽΪ �� ������SO2��NaOH��Һ��Ӧ�����ӷ���ʽΪ ��
��2�����ܼ����������о��豣�������������Ŀ���������Ԫ�صĽ����ʺ� ��
�������漰��Ӧ�����ӷ���ʽΪ ��
��3��ͨ��������ʱ����������Ҫ��Ӧ�����ӷ���ʽΪ ���ù��̲�����β�����ü���Һ���գ�β������Ⱦ����������Ϊ ��д��ѧʽ����
���𰸡�
��12�֣�
��1�� 4FeS2+11O2=2Fe2O3+8SO2 SO2��2OH-��SO32��+2 H2O
��2��
����Fe3��ˮ�� Fe3����3H2O 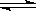 Fe��OH��3+3H��
Fe��OH��3+3H��
��3�� Cl2��2Fe2����2Cl����2Fe3�� Cl2 HCl
��������

��ϰ��ϵ�д�
�����Ŀ

 2SO3(g)���÷�Ӧ��ƽ�ⳣ������ʽΪK�� ��������SO2��NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ ��
2SO3(g)���÷�Ӧ��ƽ�ⳣ������ʽΪK�� ��������SO2��NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ �� ��2�����ܼ����������о��豣�������������Ŀ����
��
��
��2�����ܼ����������о��豣�������������Ŀ����
��
��
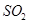 ת��Ϊ
ת��Ϊ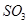 �ķ�ӦΪ
�ķ�ӦΪ ���÷�Ӧ��ƽ�ⳣ������ʽΪK= ��������
���÷�Ӧ��ƽ�ⳣ������ʽΪK= ��������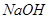 ��Һ��Ӧ�Ļ�ѧ����ʽΪ
��Һ��Ӧ�Ļ�ѧ����ʽΪ