题目内容
把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含amol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁:另一份加入含bmol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的物质的量浓度为 ( )
| A.(b-a) /V mol·L-1 | B.(2b-a)/V mol·L-1 | C.2(b-a)/V mol·L-1 | D.2(2b-a)/V mol·L-1 |
D
解:硫酸镁与氢氧化钠反应的方程式为: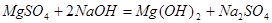 ,所以
,所以 L混合溶液中
L混合溶液中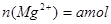 ;硫酸根离子与钡离子反应的离子方程式为:
;硫酸根离子与钡离子反应的离子方程式为: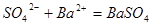 ,所以
,所以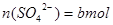 ;由于
;由于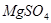 中
中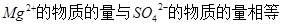 ;所以K2SO4中的硫酸根离子的物质的量为
;所以K2SO4中的硫酸根离子的物质的量为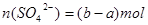 ,即
,即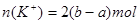 ,所以,原混合溶液中钾离子的物质的量浓度为2(2b-a)/V mol·L-1
,所以,原混合溶液中钾离子的物质的量浓度为2(2b-a)/V mol·L-1
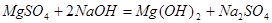 ,所以
,所以 L混合溶液中
L混合溶液中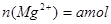 ;硫酸根离子与钡离子反应的离子方程式为:
;硫酸根离子与钡离子反应的离子方程式为: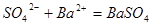 ,所以
,所以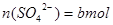 ;由于
;由于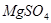 中
中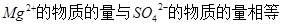 ;所以K2SO4中的硫酸根离子的物质的量为
;所以K2SO4中的硫酸根离子的物质的量为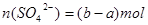 ,即
,即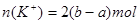 ,所以,原混合溶液中钾离子的物质的量浓度为2(2b-a)/V mol·L-1
,所以,原混合溶液中钾离子的物质的量浓度为2(2b-a)/V mol·L-1
练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
 、 。
、 。
 氧化钠固体,C.浓氨水,D.浓硫酸,E.碳酸氢铵。采用“套管法”,只用一支试管(药匙等辅助用品略,不加热),选择合适的药品就可在圆底烧瓶中集满喷泉实验用的氨气(如图丙)。
氧化钠固体,C.浓氨水,D.浓硫酸,E.碳酸氢铵。采用“套管法”,只用一支试管(药匙等辅助用品略,不加热),选择合适的药品就可在圆底烧瓶中集满喷泉实验用的氨气(如图丙)。 00 mL NaOH溶液中缓慢通入一定量的CO2气体,充分反应后,测得最后所得溶液M的pH>7(反应前后溶液的体积变化忽略不计)。在溶液M中逐滴缓慢滴加1 mol/L盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
00 mL NaOH溶液中缓慢通入一定量的CO2气体,充分反应后,测得最后所得溶液M的pH>7(反应前后溶液的体积变化忽略不计)。在溶液M中逐滴缓慢滴加1 mol/L盐酸,所得气体的体积与所加盐酸的体积关系如图所示:

 原混合液中Na2SO4的物质的量浓度。
原混合液中Na2SO4的物质的量浓度。