题目内容
【题目】下图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质被略去。反应①常被应用于野外焊接钢轨,F是海水中含有盐的主要成分,J为D、G反应产物形成的水溶液。
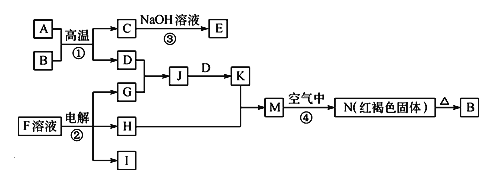
请回答下列问题:
(1)B的化学式为 。
(2)H的电子式为 。
(3)写出反应②的离子方程式 。
(4)写出反应④的化学方程式 。
(5)D是目前应用最广泛的金属,D与炭混合物在水溶液中可形成许多微电池。将含有Cr2O72–的酸性废水通过该混合物,在微电池 极上Cr2O72–转化为Cr3+,其电极反应式为 。
【答案】(1)Fe2O3
(2)![]()
(3)![]()
(4)4Fe(OH)2+O2+2H2O=4Fe(OH)3
(5)正 Cr2O72–+6e-+14H+ = 2Cr3++7H2O
【解析】
试题分析:F是海水中含有盐的主要成分,F是氯化钠,氯化钠溶液电解生成氢气、氯气、氢氧化钠;铁与G反应,所以G是氯气、H是水;N是红褐色固体,N是氢氧化铁,B是氧化铁;反应①常被应用于野外焊接钢轨,A为铝;C与氢氧化钠反应,C是氧化铝;E是偏铝酸钠;M在空气中生成氢氧化铁,M是氯化亚铁;(1)B的化学式为Fe2O3。
(2)水的电子式为![]()
(3)电解氯化钠溶液的离子方程式![]() 。
。
(4)氢氧化亚铁被氧化为氢氧化铁的化学方程式4Fe(OH)2+O2+2H2O=4Fe(OH)3。
(5)铁与炭混合物在水溶液中可形成许多微电池。将含有Cr2O72–的酸性废水通过该混合物,Cr2O72–转化为Cr3+是还原反应,在微电池正极极上,其电极反应式为Cr2O72–+6e-+14H+ = 2Cr3++7H2O。

练习册系列答案
相关题目