题目内容
设NA表示阿伏加德罗常数,下列叙述中正确的是
| A.标准状况下,2.24 L CCl4所含的原子数为0.5 NA |
| B.100 m L 0.1 mol/L的NaCl 溶液中,所含微粒总数为0.02 NA |
| C.1.7 g的OH-中含有的电子数为NA |
| D.78 g Na2O2与足量水反应转移电子数为2 NA |
C
试题分析:A.标准状况下,CCl4是液体,其摩尔体积不为22.4L,故2.24 L CCl4所含的原子数不为0.5 NA,故错误。B. 100 m L 0.1 mol/L的 NaCl 溶液的物质的量为0.1×0.1=0.01mol,溶液中含有的微粒为Na+、Cl-、H+、OH-、NaCl、H2O等,含有的微粒数不为0.02 NA,故错误。C.OH-的相对分子质量为17g/mol,1.7gOH-的物质的量为0.1mol,1molO原子含有8mol电子,1molH原子含有1mol电子,1molOH-基团本身含有1mol负电荷,因此1molOH-含有10mol电子,故0.1molOH-含有的电子数为NA,故正确。D. Na2O2的相对分子质量为78g/mol,78 g Na2O2为1mol,与水反应的方程式为:2Na2O2+2H2O= 4NaOH+O2↑,1mol Na2O2转移电子1mol,因此转移电子数为NA。故错误。

练习册系列答案
相关题目
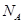 表示阿伏加德罗常数,下列说法中正确的是
表示阿伏加德罗常数,下列说法中正确的是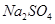 的溶液中含
的溶液中含
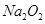 固体中含2
固体中含2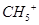 离子所含电子数为10
离子所含电子数为10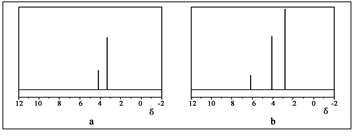
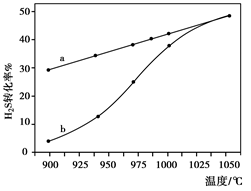
 H2(g)+1/2S2(g) 在恒容密闭容器中,控制不同温度进行H2S的分解实验:以H2S的起始浓度均为c mol·L-1测定H2S的转化率,结果如右下图所示。图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。若985℃时,反应经t min达到平衡,此时H2S的转化率为40%,则反应速率v(H2)= (用含c、t的代数式表示)。请说明随温度的升高,曲线b向曲线a逼近的原因: 。
H2(g)+1/2S2(g) 在恒容密闭容器中,控制不同温度进行H2S的分解实验:以H2S的起始浓度均为c mol·L-1测定H2S的转化率,结果如右下图所示。图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。若985℃时,反应经t min达到平衡,此时H2S的转化率为40%,则反应速率v(H2)= (用含c、t的代数式表示)。请说明随温度的升高,曲线b向曲线a逼近的原因: 。