题目内容
下列叙述中正确的是( )A.原子晶体中可能含有共价键,离子晶体一定含有离子键
B.NaCl固体中因为有Na+和Cl-所以能导电
C.气态氢化物的熔沸点:HF>HCl>HBr>HI
D.有新单质生成的化学反应不一定都是氧化-还原反应
【答案】分析:A.原子晶体中一定含有共价键;
B.氯化钠固体中含有阴阳离子,但氯化钠固体不导电;
C.分子晶体中,气态氢化物的熔沸点与其相对分子质量成正比,但氢键影响氢化物的熔沸点;
D.有单质生成的化学反应不一定都是氧化还原反应.
解答:解:A.原子晶体中一定含有共价键,离子晶体一定含有离子键,故A错误;
B.氯化钠固体中含有阴阳离子,但阴阳离子不能自由移动,所以氯化钠固体不能导电,故B错误;
C.分子晶体中,气态氢化物的熔沸点与其相对分子质量成正比,但氢键影响氢化物的熔沸点,所以卤元素的氢化物中氟化氢的熔沸点大于氯化氢,故C错误;
D.有单质生成的化学反应不一定都是氧化还原反应,如石墨和金刚石之间的转化,故D正确;
故选D.
点评:本题考查较综合,根据晶体的构成、物质导电的原因、分子晶体熔沸点高低的判断、氧化还原反应的特征来分析解答即可,易错选项是D,注意特殊情况,为易错题.
B.氯化钠固体中含有阴阳离子,但氯化钠固体不导电;
C.分子晶体中,气态氢化物的熔沸点与其相对分子质量成正比,但氢键影响氢化物的熔沸点;
D.有单质生成的化学反应不一定都是氧化还原反应.
解答:解:A.原子晶体中一定含有共价键,离子晶体一定含有离子键,故A错误;
B.氯化钠固体中含有阴阳离子,但阴阳离子不能自由移动,所以氯化钠固体不能导电,故B错误;
C.分子晶体中,气态氢化物的熔沸点与其相对分子质量成正比,但氢键影响氢化物的熔沸点,所以卤元素的氢化物中氟化氢的熔沸点大于氯化氢,故C错误;
D.有单质生成的化学反应不一定都是氧化还原反应,如石墨和金刚石之间的转化,故D正确;
故选D.
点评:本题考查较综合,根据晶体的构成、物质导电的原因、分子晶体熔沸点高低的判断、氧化还原反应的特征来分析解答即可,易错选项是D,注意特殊情况,为易错题.

练习册系列答案
相关题目
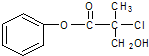 有机物A是农药生产中的一种中间体,结构简式如图所示.下列叙述中正确的是( )
有机物A是农药生产中的一种中间体,结构简式如图所示.下列叙述中正确的是( )| A、有机物A可以在一定条件下与HBr发生反应 | B、1mol A最多能与4mol H2发生加成反应 | C、有机物A与浓硫酸混合加热,可以发生消去反应 | D、1mol A与足量的NaOH溶液反应,最多可以消耗3mol NaOH |


