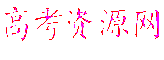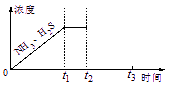题目内容
26.脱除天然气中的硫化氢既能减少环境污染,又可回收硫资源。(1)硫化氢与FeCl3溶液反应生成单质硫,其离子方程式为 。
(2)用过量NaOH溶液吸收硫化氢后,以石墨作电极电解该溶液可回收硫,其电解总反应方程式(忽略氧的氧化还原)为 ;该方法的优点是 。
(3)一定温度下1 mol NH4 HS固体在定容真空容器中可部分分解为硫化氢和氨气。
①当反应达平衡时ρ氨气×p硫化氢=a(Pa2),则容器中的总压为 Pa;
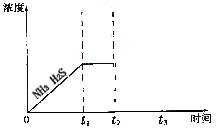
②题26图是上述反应过程中生成物浓度随时间变化的示意图。若t2时增大氨气的浓度且在t3时反应再次达到平衡,请在图上画出t2时刻后氨气、硫化氢的浓度随时间的变化曲线.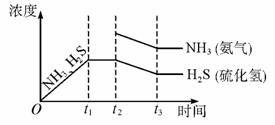
题26图
(1)2Fe3++H2S=S↓+2Fe2++2H+
(2)Na2S+2H2O![]() S↓+H2↑+2NaOH或S2++2H2O
S↓+H2↑+2NaOH或S2++2H2O![]() S↓+ H2↑+2OH-
S↓+ H2↑+2OH-
副产氢气,生成的NaOH可循环利用.
(3) ①![]()
②

解析:
用(2)中方法回收硫,生成H2,对环境无污染,生成的NaOH可以循环利用,体现了环保节能的原则。
(3)中发生的反应:NH4HS(s)![]() NH3(g)+H2S(g),容器中,p(NH3)·p(H2S)=a(Pa2)。而向容器中加入NH3时,c(NH3)增大,该平衡体系向逆方向移动,保持c(H2S)与c(NH3)均减小。
NH3(g)+H2S(g),容器中,p(NH3)·p(H2S)=a(Pa2)。而向容器中加入NH3时,c(NH3)增大,该平衡体系向逆方向移动,保持c(H2S)与c(NH3)均减小。

练习册系列答案
相关题目
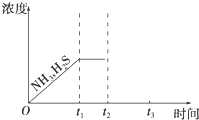 脱除天然气中的硫化氢既能减少环境污染,又可回收硫资源.
脱除天然气中的硫化氢既能减少环境污染,又可回收硫资源.