题目内容
【题目】镁—次氯酸盐燃料电池的工作原理如右图所示,该电池反应为:
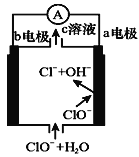
Mg+ClO-+H2O=Mg(OH)2+Cl-
下列有关说法正确的是( )
A.电池工作时,c溶液中的溶质是MgCl2
B.负极反应式:ClO--2e-+H2O=Cl-+2OH-
C.电池工作时,OH-向b电极移动
D.b电极发生还原反应,每转移0.1 mol电子,理论上生成0.1 mol Cl-
【答案】C
【解析】
试题分析:A、根据电池的装置示意图,ClO-→Cl-,化合价降低,得电子,根据原电池的工作原理,a极为正极,b极为负极,正极反应式为ClO-+H2O+2e-=Cl-+2OH-,负极反应式为Mg+2OH--2e-=Mg(OH)2↓,因此c溶液不是MgCl2,故错误;B、根据选项A的分析,负极反应式为Mg+2OH--2e-=Mg(OH)2↓,故错误;C、根据原电池的工作原理,阴离子向负极移动,阳离子向正极移动,因此OH-向b极移动,故正确;D、根据上述分析,b极失去电子,化合价升高,发生氧化反应,故错误。

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目