题目内容
【题目】科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇和水,并开发出以甲醇为燃料的燃料电池.已知图甲池为甲醇燃
料电池;乙池中的两个电极均为石墨电极,乙池中盛有100mL 3.00mol.L﹣1的CuSO4溶液.请回答下列问题: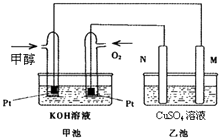
(1)M的电极反应式为
(2)当乙池中某一电极析出金属铜6.4g时,甲池中理论上消耗氧气为多少L.(标准状况)
(3)若乙池中两电极产生的气体恰好相等时(假设标准状况下),理论上需通入g甲醇.
【答案】
(1)Cu2++2e﹣=Cu
(2)1.12
(3)6.4
【解析】解:(1)燃料电池的正极上是氧气发生得电子的还原反应,电解池中,和电源的正极相连的是阳极,该极上发生氧化反应,所以N是阳极,M是阴极,M极上电极反应为:Cu2++2e﹣=Cu,所以答案是:Cu2++2e﹣=Cu;
(2.)乙池中M电极析出金属铜6.4g,根据电极反应:Cu2++2e﹣=Cu,析出金属铜6.4g即0.1mol,转移电子的物质的量是0.2mol,在燃料电池的正极上发生电极反应:
O2+2H2O+4e﹣=4OH﹣ , 当转移电子的物质的量是0.2mol时,消耗氧气的物质的量是0.05mol,体积是0.05mol×22.4L/mol=1.12L,
所以答案是:1.12;
(3.)乙池中发生的反应分别是:阳极上:4OH﹣=O2↑+2H2O+4e﹣ , 阳极上Cu2++2e﹣=Cu,2H++2e﹣=H2↑,100mL3.00molL﹣1的CuSO4溶液中铜离子物质的量是:0.3mol,铜离子得电子的是0.6mol,若两电极产生的气体恰好相等时(假设标准状况下),设均为nmol,则2n+0.6=4n,解得n=0.3,即装置在转移电子的物质的量是1.2mol,甲醇燃料电池的负极上发生反应:CH3OH+8OH﹣﹣6e﹣=CO32﹣+6H2O,当转移电子是1.2mol,消耗甲醇的物质的量是0.2mol,质量是0.2mol×32g/mol=6.4g,
所以答案是:6.4.