题目内容
(8分)某兴趣小组根据金属镁与C02的反应,推测金属钠也能与C02发生反应,因此
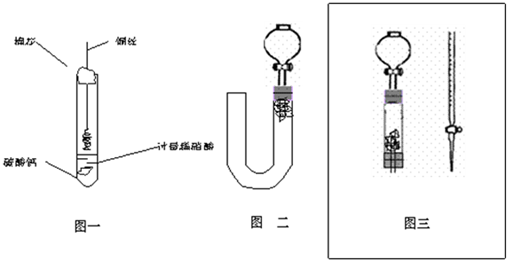
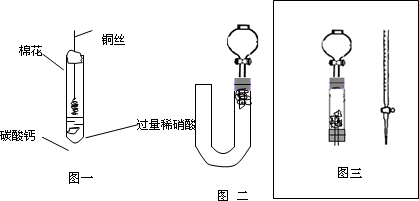
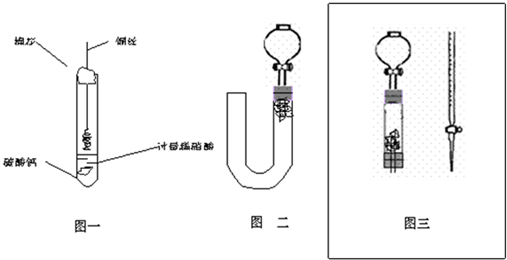
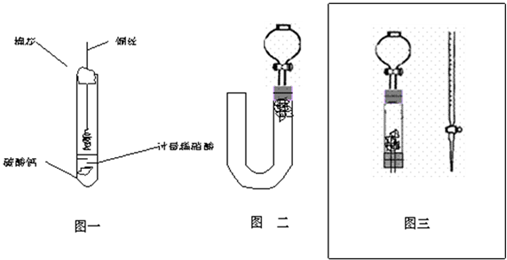
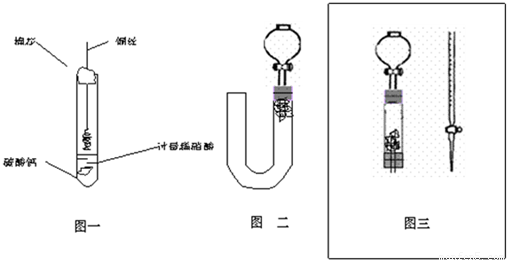
他们用下图所示的装置进行“钠与C02反应”的探究(尾气处理装置略去).又知实
验过程中的C02气体为足量;设能发生的反应都进行完全;一氧化碳气体可用氯化钯
(PdCl2)溶液来检验(通过溶液颜色的变化来判断)。
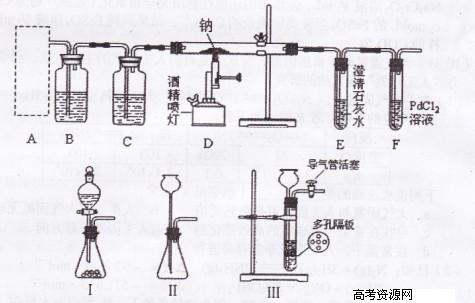
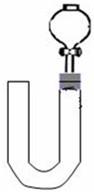
(1)为了使制取气体的装置能“随开随用,随关随停”,则在图中A处应选用的装置是 (填“I”、“Ⅱ”或“Ⅲ”).若要用干燥、纯净的C02气体与金属钠反应,则装置B中应盛放的试剂是 溶液。
(2)实验开始,检查装置的气密性完好并装入有关药品后,在点燃酒精喷灯前,还必须进行的实验操作是 。
(3)反应完成后,装置D玻璃管中残留的固体物质可能是 。(填字母)
![]() .Na202 b.Na2C03 c.NaHCO3 d.Na2C03和C
.Na202 b.Na2C03 c.NaHCO3 d.Na2C03和C
(4)若D玻璃管中残留的固体是纯净物,则钠与C02反应的化学方程式是 。
(5)请设计合理的实验来检验某固体物质是Na2C03.答: 。
共8分。第(4)、(5)题各2分,其余每空1分。
(1)Ⅲ 饱和NaHCO3 (2)打开Ⅲ的导气管活塞(先通一会CO2气) (3)b
(4)2Na +2CO2![]() Na2CO3 + CO
Na2CO3 + CO
(5)取少量固体进行焰色反应,火焰呈黄色。再取少量固体跟适量CaCl2溶液反应,有白色沉淀生成。取少量固体跟稀盐酸反应,产生无色无味气体

练习册系列答案
相关题目