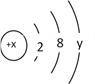��Ŀ����
����Ŀ��������������(Na2S2O4)��ӡȾ��ҵ��һ�ֳ���ԭ�����������������ֳƱ��շۣ�������ˮ���������ڼ״�����������ȡ���ˮ���ᷢ����Ӧ�ų��������ȣ���������ȼ�գ���ҵ�Ʊ��������£�
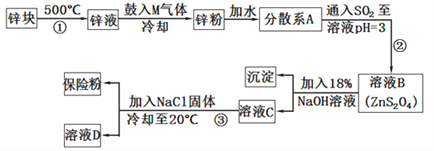
��ش��������⣺
��1�����������������Ƶ�ע������_____________________(��дһ��)��
��2����Һп�й���M���壬ʹҺ̬п������Ŀ����___________________�����������MΪ������һ����Ҫ�ɷ֣���M�ĵ���ʽΪ________________��
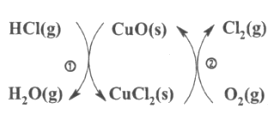
��3���������Ļ�ѧ����ʽΪ________________________________________________��
��4���������ķ��뷽������Ϊ���ˡ�ϴ�ӡ����������й����õ��IJ����������ձ������������________��ϴ�������Լ���_______��ʵ��ʱ����NaCl�����������____________________________��
��5�������������ƿ������ڳ�ȥ��ˮ�е��ظ��������(Cr2O72-��ת��ΪCr3+��S2O42-��ת��ΪSO42-)��д���÷�Ӧ�����ӷ���ʽ__________________________________��
���𰸡� �ܷ⡢����������(������������) ����п��Ӧ�ı����ף��ӿ컯ѧ��Ӧ���� ![]() Zn+2SO2 = ZnS2O4 ©�� �״� ����Na2S2O4���ܽ�Ȼ�����Na+Ũ�ȣ�����Na2S2O4�ᾧ���� Cr2O72-+S2O42-+6H+ = 2Cr3+ +2SO42- +3H2O
Zn+2SO2 = ZnS2O4 ©�� �״� ����Na2S2O4���ܽ�Ȼ�����Na+Ũ�ȣ�����Na2S2O4�ᾧ���� Cr2O72-+S2O42-+6H+ = 2Cr3+ +2SO42- +3H2O
����������1����Ϊ��Ŀ�й��ڱ��շ�˵��Ϊ����������ȡ���ˮ���ᷢ����Ӧ�ų��������ȣ���������ȼ�ա����Ա���ʱӦ���ܷⱣ�棬�������ȣ�ͬʱҲӦ����������ȼ����롣
��2����Һп�й���M���壬ʹҺ̬п������Ŀ���Ǽ�Сп�Ŀ�����ʹ����п�ı�����������������뷴Ӧ��ĽӴ�������ӿ췴Ӧ���ʡ����������MΪ������һ����Ҫ�ɷ֣���Mֻ���ǵ����������ʽΪ![]() ��
��
��3�����̢ڵ�Ŀ���ǽ�����пת��ΪZnS2O4��������Zn����ͨ��SO2���仯ѧ����ʽΪ��Zn+2SO2 = ZnS2O4��
��4������ʹ�õIJ�������Ϊ�ձ�����������©����ϴ�Ӳ�Ʒʱ�����ǵ���Ŀ�ж��ڱ��շ۵�������������ˮ���������ڼ״��������ü״�ϴ���Է�ֹ��Ʒ����ʧ��ʵ���м����Ȼ��Ƶ�Ŀ��������ͬ����ЧӦ������Na2S2O4���ܽ�����Ա�����������
��5�������������ƿ������ڳ�ȥ��ˮ�е��ظ��������(Cr2O72-��ת��ΪCr3+��S2O42-��ת��ΪSO42-)�����ϵõ����ַ�Ӧ��Cr2O72-+S2O42- �� Cr3+ +SO42-��Cr2O72-���ϼ۽���6����2��Cr��ÿ������3�ۣ���S2O42-���ϼ�����6����2��S��ÿ������3�ۣ��������������ӵ�ϵ������1������ʽ��ΪCr2O72-+S2O42- �� 2Cr3+ + 2SO42-���ٸ���ԭ�Ӹ����غ�͵���غ�õ���Cr2O72-+S2O42-+6H+ = 2Cr3+ +2SO42- +3H2O��

 ϰ�⾫ѡϵ�д�
ϰ�⾫ѡϵ�д�����Ŀ������ͼ��ʾװ�ý�������ʵ�飬ʵ������Ԥ���������һ������
ѡ�� | �� | �� | ���� |
A | ����KI��Һ | Ũ���� | ��Һ���� |
B | ��̪��Һ | Ũ���� | �����Ա仯 |
C | AlCl3��Һ | Ũ��ˮ | �а�ɫ���� |
D | Ũ���� | Ũ��ˮ | �а��̲��� |
A. A B. B C. C D. D
����Ŀ����300mL���ܱ������У��������۲�����һ������CO���壬һ�������·�����Ӧ��Ni��s��+4CO��g��Ni��CO��4��g������֪�÷�Ӧƽ�ⳣ�����¶ȵĹ�ϵ�����
�¶�/�� | 25 | 80 | 230 |
ƽ�ⳣ�� | 5��104 | 2 | 1.9��10��5 |
����˵������ȷ���ǣ�������
A.��������Ni��CO��4��g���ķ�ӦΪ���ȷ�Ӧ
B.25��ʱ��ӦNi��CO��4��g��Ni��s��+4CO��g����ƽ�ⳣ��Ϊ2��10��5
C.80��ﵽƽ��ʱ�����n��CO��=0.3mol����Ni��CO��4��ƽ��Ũ��Ϊ2 mol/L
D.��80��ʱ�����ijʱ�̣�Ni��CO��4��COŨ�Ⱦ�Ϊ0.5 mol/L�����ʱv��������v���棩