��Ŀ����
��10�֣���֪������ء����������������������ܽ�������(Na2C2O4)������
MnO4����C2O42����H���D��Mn2����CO2����H2O(δ��ƽ)��
MnO2��C2O42����H���D��Mn2����CO2����H2O(δ��ƽ)��
Ϊ�ⶨij���̿��ж������̵�����������ȷ����1.20 g���̿���Ʒ������2.68 g�����ƹ��壬�ټ���������ϡ���Ტ����(���ʲ��μӷ�Ӧ)����ַ�Ӧ����ȴ����������Һת�Ƶ�����ƿ��������ˮϡ�����̶ȣ�����ȡ��25.0 mL����0.0200 mol��L��1���������Һ���еζ���������20.0 mL��Һʱǡ����ȫ��Ӧ���Ը���������Ϣ������и��⣺
(1)��ƽ�����������ӷ���ʽ��
___MnO��___C2O��___H��===___Mn2����___CO2����___H2O��
___MnO2��__C2O��___H��===___Mn2����___CO2����__H2O��
(2)��������̿��ж������̵�������������ȱһ�����ݣ����������__________(������������������)��
(3)�������ݵ���ֵΪ250��������̿��ж������̵���������(д���������)����4�֣�
MnO4����C2O42����H���D��Mn2����CO2����H2O(δ��ƽ)��
MnO2��C2O42����H���D��Mn2����CO2����H2O(δ��ƽ)��
Ϊ�ⶨij���̿��ж������̵�����������ȷ����1.20 g���̿���Ʒ������2.68 g�����ƹ��壬�ټ���������ϡ���Ტ����(���ʲ��μӷ�Ӧ)����ַ�Ӧ����ȴ����������Һת�Ƶ�����ƿ��������ˮϡ�����̶ȣ�����ȡ��25.0 mL����0.0200 mol��L��1���������Һ���еζ���������20.0 mL��Һʱǡ����ȫ��Ӧ���Ը���������Ϣ������и��⣺
(1)��ƽ�����������ӷ���ʽ��
___MnO��___C2O��___H��===___Mn2����___CO2����___H2O��
___MnO2��__C2O��___H��===___Mn2����___CO2����__H2O��
(2)��������̿��ж������̵�������������ȱһ�����ݣ����������__________(������������������)��
(3)�������ݵ���ֵΪ250��������̿��ж������̵���������(д���������)����4�֣�
��10�֣� (1)2��5��16��2��10��8��
�� 1��1��4��1��2��2
(2)����ƿ���ݻ�
(3)
 ��
��
�ζ�250 mLϡ�ͺ����Һ������n(MnO4��)��0.0200 mol��L��1��0.02 L��10��0.004 mol��
����������ԭ��Ӧ�е�ʧ��������ȣ���
n(MnO2)��2��0.004 mol��5��0.02 mol��2��
n(MnO2)��0.01 mol��
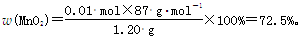
�� 1��1��4��1��2��2
(2)����ƿ���ݻ�
(3)
 ��
���ζ�250 mLϡ�ͺ����Һ������n(MnO4��)��0.0200 mol��L��1��0.02 L��10��0.004 mol��
����������ԭ��Ӧ�е�ʧ��������ȣ���
n(MnO2)��2��0.004 mol��5��0.02 mol��2��
n(MnO2)��0.01 mol��
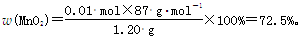
(1)��ѧ����ʽ����ƽ��Mn +7��+2�ۣ�C��+3��+4�ۣ����Ϊ2��5��16��2��10��8��
Mn +4��+2�ۣ�C��+3��+4�ۣ����Ϊ1��1��4��1��2��2
(2)����ƿ���ݻ���������ȷ��ȡ������Һ��Ũ�ȡ�
(3)
 ��
���ζ�250 mLϡ�ͺ����Һ������n(MnO4��)��0.0200 mol��L��1��0.02 L��10��0.004 mol��
����������ԭ��Ӧ�е�ʧ��������ȣ���
n(MnO2)��2��0.004 mol��5��0.02 mol��2��
n(MnO2)��0.01 mol��
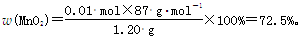

��ϰ��ϵ�д�
�����Ŀ
 NH3��H��
NH3��H��
 ������ˮ��Ӧ��Fe3++3NH3��H2O=F��OH��3��+3NH4+
������ˮ��Ӧ��Fe3++3NH3��H2O=F��OH��3��+3NH4+ ��2H��
��2H�� H2O��CO2��
H2O��CO2�� ����������Һ�м�������ҺBa2����SO
����������Һ�м�������ҺBa2����SO
 ��
��