题目内容
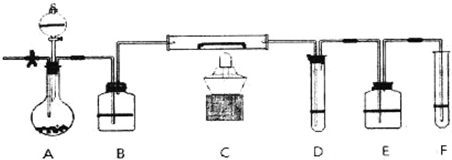
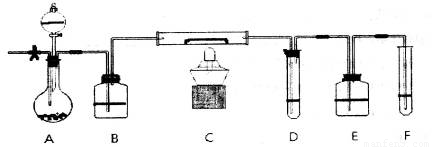
A装置中装有淡黄色的固体,分液漏斗中装有浓盐酸,B中盛浓硫酸,C中放有催化剂,D中盛淀粉碘化钾溶液,E中盛足量的NaOH溶液,F中盛FeSO4和H2SO4混合溶液.
先打开止水夹,通入N2,待装置中空气被赶尽后关闭止水夹,点燃酒精灯:从分液漏斗放入浓盐酸,D中溶液迅速变蓝,F中溶液由浅绿色变为棕黄色(整个装置无O3).
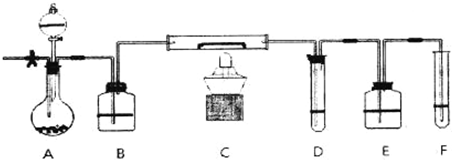
(1)淡黄色固体所含化学键的名称为:______;装有遮黄色的固体仪器的名称______.
(2)如何检查装置的气密性______.
(3)C中反应的化学方程式______.
(4)E装置中反应的离子方程式______.
(5)如F中仍有Fe2+,如何检验含有Fe2+______.
解:(1)A装置中装有淡黄色的固体,应为Na2O2,含有离子键和共价键,装有遮黄色的固体仪器的名称为圆底烧瓶,
故答案为:离子键、共价键;圆底烧瓶;
(2)检验气密性,可关闭止水夹,将F中的导管伸入水槽中,用酒精灯给圆底烧瓶微热,导管口有气泡产生,冷却后,导管出现水柱,
故答案为:关闭止水夹,将F中的导管伸入水槽中,用酒精灯给圆底烧瓶微热,导管口有气泡产生,冷却后,导管出现水柱;
(3)C中发生4HCl+O2 2Cl2+2H2O,故答案为:4HCl+O2
2Cl2+2H2O,故答案为:4HCl+O2 2Cl2+2H2O;
2Cl2+2H2O;
(4)E中盛足量的NaOH溶液,通入氯气发生:Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
(5)Fe2+可与高锰酸钾溶液发生氧化还原反应,检验Fe2+,可取F中少量溶液于小试管中,滴加一滴高锰酸钾溶液,高锰酸钾溶液褪色,说明含有Fe2+.
故答案为:取F中少量溶液于小试管中,滴加一滴高锰酸钾溶液,高锰酸钾溶液褪色,说明含有Fe2+.
分析:A装置中装有淡黄色的固体,应为Na2O2,在圆底烧瓶中与水反应生成氧气,并放热,则从A中出来的气体为氧气和HCl的混合物,经浓硫酸干燥后在C中发生4HCl+O2 2Cl2+2H2O,氯气可与KI发生氧化还原反应生成I2,D中含有淀粉,遇碘变蓝色,F中盛FeSO4和H2SO4混合溶液,由浅绿色变为棕黄色,发生2Fe2++Cl2=2Fe3++2Cl-,以此解答该题.
2Cl2+2H2O,氯气可与KI发生氧化还原反应生成I2,D中含有淀粉,遇碘变蓝色,F中盛FeSO4和H2SO4混合溶液,由浅绿色变为棕黄色,发生2Fe2++Cl2=2Fe3++2Cl-,以此解答该题.
点评:本题考查氧气的制备以及氧气和HCl在催化作用下反应的性质探究,侧重于学生实验能力和考查,注意把握实验原理和基本实验操作方法,题目难度不大.
故答案为:离子键、共价键;圆底烧瓶;
(2)检验气密性,可关闭止水夹,将F中的导管伸入水槽中,用酒精灯给圆底烧瓶微热,导管口有气泡产生,冷却后,导管出现水柱,
故答案为:关闭止水夹,将F中的导管伸入水槽中,用酒精灯给圆底烧瓶微热,导管口有气泡产生,冷却后,导管出现水柱;
(3)C中发生4HCl+O2
 2Cl2+2H2O,故答案为:4HCl+O2
2Cl2+2H2O,故答案为:4HCl+O2 2Cl2+2H2O;
2Cl2+2H2O;(4)E中盛足量的NaOH溶液,通入氯气发生:Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
(5)Fe2+可与高锰酸钾溶液发生氧化还原反应,检验Fe2+,可取F中少量溶液于小试管中,滴加一滴高锰酸钾溶液,高锰酸钾溶液褪色,说明含有Fe2+.
故答案为:取F中少量溶液于小试管中,滴加一滴高锰酸钾溶液,高锰酸钾溶液褪色,说明含有Fe2+.
分析:A装置中装有淡黄色的固体,应为Na2O2,在圆底烧瓶中与水反应生成氧气,并放热,则从A中出来的气体为氧气和HCl的混合物,经浓硫酸干燥后在C中发生4HCl+O2
 2Cl2+2H2O,氯气可与KI发生氧化还原反应生成I2,D中含有淀粉,遇碘变蓝色,F中盛FeSO4和H2SO4混合溶液,由浅绿色变为棕黄色,发生2Fe2++Cl2=2Fe3++2Cl-,以此解答该题.
2Cl2+2H2O,氯气可与KI发生氧化还原反应生成I2,D中含有淀粉,遇碘变蓝色,F中盛FeSO4和H2SO4混合溶液,由浅绿色变为棕黄色,发生2Fe2++Cl2=2Fe3++2Cl-,以此解答该题.点评:本题考查氧气的制备以及氧气和HCl在催化作用下反应的性质探究,侧重于学生实验能力和考查,注意把握实验原理和基本实验操作方法,题目难度不大.

练习册系列答案
相关题目

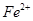 ,如何检验含有Fe2+____________________________________。
,如何检验含有Fe2+____________________________________。