题目内容
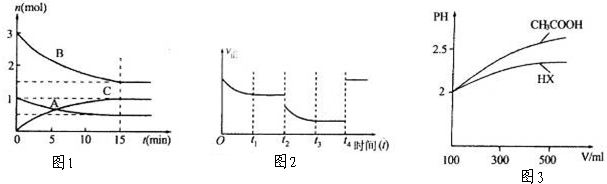
(1)常温下有pH分别为8、9、10的三种相同物质的量浓度的盐溶液NaX、NaY、NaZ,比较盐酸、HX、HY、HZ四种酸酸性由强到弱
(2)已知25℃时:H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ?mol-1
氢氟酸是一种弱酸,可用来刻蚀玻璃.20mL 0.1mol?L-1的氢氟酸与0.1mol/L氢氧化钠溶液完全反应时放热akJ,写出氢氟酸电离的热化学方程式
HCl>HX>HY>HZ
HCl>HX>HY>HZ
(2)已知25℃时:H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ?mol-1
氢氟酸是一种弱酸,可用来刻蚀玻璃.20mL 0.1mol?L-1的氢氟酸与0.1mol/L氢氧化钠溶液完全反应时放热akJ,写出氢氟酸电离的热化学方程式
HF?H++F-,△H=+(57.3-0.5a)kJ/mol
HF?H++F-,△H=+(57.3-0.5a)kJ/mol
.分析:(1)酸的酸性越强,其酸根离子的水解程度越小,则相同浓度钠盐溶液的pH越小;
(2)氢氟酸是弱电解质,弱电解质的电离过程要吸收热量,然后根据盖斯定律写出氢氟酸电离的热化学反应方程式.
(2)氢氟酸是弱电解质,弱电解质的电离过程要吸收热量,然后根据盖斯定律写出氢氟酸电离的热化学反应方程式.
解答:解:(1)酸的酸性越强,其酸根离子的水解程度越小,则相同浓度钠盐溶液的pH越小,则相同条件下的钠盐溶液,溶液的pH越大的其相应酸的酸性越小,根据题意知,这三种酸的酸性大小顺序是HX、HY、HZ,盐酸是强酸,其酸性最强,则这四种酸的酸性大小顺序是HCl>HX>HY>HZ,
故答案为:HCl>HX>HY>HZ;
(2)氢氟酸是弱电解质,弱电解质的电离过程要吸收热量,
20mL 0.1mol/L的氢氟酸与0.1mol/L氢氧化钠溶液完全反应时放热a kJ,则1molHF和氢氧化钠溶液完全反应时放出的热量=
=0.5kJ,
根据盖斯定律知,1molHF电离吸收的热量=+(57.3-0.5a)kJ/mol,
则氢氟酸的电离热化学方程式为:HF?H++F-,△H=+(57.3-0.5a)kJ/mol,
故答案为:HF?H++F-,△H=+(57.3-0.5a)kJ/mol.
故答案为:HCl>HX>HY>HZ;
(2)氢氟酸是弱电解质,弱电解质的电离过程要吸收热量,
20mL 0.1mol/L的氢氟酸与0.1mol/L氢氧化钠溶液完全反应时放热a kJ,则1molHF和氢氧化钠溶液完全反应时放出的热量=
| a×10-3kJ |
| 0.1mol/L×0.02L |
根据盖斯定律知,1molHF电离吸收的热量=+(57.3-0.5a)kJ/mol,
则氢氟酸的电离热化学方程式为:HF?H++F-,△H=+(57.3-0.5a)kJ/mol,
故答案为:HF?H++F-,△H=+(57.3-0.5a)kJ/mol.
点评:本题考查盐类的水解、热化学方程式的书写等知识点,明确酸的强弱与其酸根离子水解能力大小的关系是解本题关键,难度不大.

练习册系列答案
相关题目
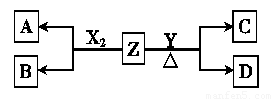
 (1)写出常温下单质X2与Z反应的离子方程式
(1)写出常温下单质X2与Z反应的离子方程式