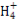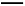题目内容
用Pt作电极,电解含c(Cu2+)∶c(Na+)∶c(Cl-)=1∶2∶4的混合溶液,在任何情况下,阴、阳两极下不可能同时发生的反应是( )
A.阴极:2H++2e-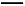 H2↑ 阳极:4OH--4e-
H2↑ 阳极:4OH--4e-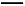 2H2O+O2↑
2H2O+O2↑
B.阴极:2H++2e-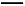 H2↑ 阳极:2Cl--2e-
H2↑ 阳极:2Cl--2e-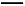 Cl2↑
Cl2↑
C.阴极:Cu2++2e-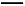 Cu 阳极:4OH--4e-
Cu 阳极:4OH--4e-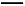 2H2O+O2↑
2H2O+O2↑
D.阴极:Cu2++2e-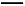 Cu 阳极:2Cl--2e-
Cu 阳极:2Cl--2e-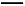 Cl2↑
Cl2↑
C
【解析】根据已知的c(Cu2+)∶c(Cl-)=1∶4可知n(Cu2+)∶n(Cl-)=1∶4。电解时阳极发生的反应首先为2Cl--2e-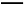 Cl2↑,其次是4OH--4e-
Cl2↑,其次是4OH--4e-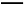 2H2O+O2↑,阴极发生的反应首先为Cu2++2e-
2H2O+O2↑,阴极发生的反应首先为Cu2++2e-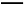 Cu,其次是2H++2e-
Cu,其次是2H++2e-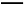 H2↑。根据Cu2+与Cl-的物质的量之比可知:当Cu2+消耗完后,Cl-还有剩余,此时阳极仍是Cl-放电,而阴极是H+放电,故C项不可能。
H2↑。根据Cu2+与Cl-的物质的量之比可知:当Cu2+消耗完后,Cl-还有剩余,此时阳极仍是Cl-放电,而阴极是H+放电,故C项不可能。

练习册系列答案
相关题目