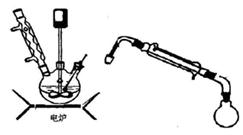
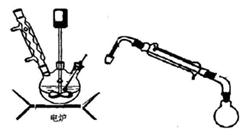
��Ŀ����
һ���¶ȷ�Χ�����Ȼ����۽��س�ʯ����Ҫ�ɷ�ΪKAlSi3O8�����Ƶ��Ȼ��أ���Ҫ��Ӧ�ǣ�NaCl��l����KAlSi3O8(s) KCl(l)��NaAlSi3O8(s)��
KCl(l)��NaAlSi3O8(s)��
��1���Ȼ��Ƶĵ���ʽ�� ��
��2��������Ӧ�漰��Ԫ���У�ԭ�Ӱ뾶������ ��
��3��������Ӧ�漰��λ��ͬһ���ڵļ���Ԫ���У���һ��Ԫ�ص�����������ˮ���������Ԫ�ص�����������ˮ������ܷ�����Ӧ����Ԫ���� ��
��4��ij��ȤС��Ϊ�о�������Ӧ�м�Ԫ�ص��۳��ʣ�Һ���м�Ԫ�ص�����ռ��Ʒ�����İٷ��ʣ����¶ȵĹ�ϵ������ʵ�飨���������������䣩������������ݣ�
|
ʱ�䣨h�� �۳��� �¶� |
1.5 |
2.5 |
3.0 |
3.5 |
4.0 |
5.0 |
|
800�� |
0.054 |
0.091 |
0.127 |
0.149 |
0.165 |
0.183 |
|
830�� |
0.481 |
0.575 |
0.626 |
0.669 |
0.685 |
0.687 |
|
860�� |
0.515 |
0.624 |
0.671 |
0.690 |
0.689 |
0.690 |
|
950�� |
0.669 |
0.714 |
0.710 |
0.714 |
0.714 |
�D�D |
�ٷ������ݿ��Եó����Ȼ����۽��س�ʯ�� ������ȡ������ȡ�����Ӧ��
��950��ʱ��������۳��ص����ʿ��Բ�ȡ�Ĵ�ʩ�� ������ţ���
a����ֽ���
b���ӳ���Ӧʱ��
c������Ӧ��ϵ��ѹǿ
d�����س�ʯ�۴�ɸ�С�Ŀ���
��5���÷����Ƶ�KCl�ᴿ�������ұ�������ء���ӦNa��l����KCl��l�� NaCl��l����K��g���ǹ�ҵ��ұ�������س��õķ�������ƽ��ԭ�����÷������е�ԭ���� ��
NaCl��l����K��g���ǹ�ҵ��ұ�������س��õķ�������ƽ��ԭ�����÷������е�ԭ���� ��
��1�� ��2��K��3��Na��4�������� ��a d ��5�����ط�������������˲����Ũ�ȣ�ƽ�������ƶ���
��2��K��3��Na��4�������� ��a d ��5�����ط�������������˲����Ũ�ȣ�ƽ�������ƶ���
��������
�����������1������д���Ȼ��Ƶĵ���ʽ�� ����2���Ƚ����Ӱ뾶���ٿ��㣬��Խ�࣬�뾶Խ��ͬ�㣬���ˣ��˵����Խ�뾶ԽС����ͬ�㡢ͬ�˿����ӣ�����Խ��뾶Խ��ԭ�Ӱ뾶������K����3��Ԫ���Ƶ�����������ˮ���������Ԫ�ص�����������ˮ������ܷ�����Ӧ����4���¶�Խ�ߣ���Ԫ�ص��۳���Խ���Ȼ����۽��س�ʯ�����ȹ��̣���950��ʱ��������۳��ص����ʿ��Բ�ȡ�Ĵ�ʩ�dz�ֽ��裬���س�ʯ�۴�ɸ�С�Ŀ������������ĽӴ��������5��������������ԭ�����ɲ�ȡ���ط�������������˲����Ũ�ȣ�ƽ�������ƶ���
����2���Ƚ����Ӱ뾶���ٿ��㣬��Խ�࣬�뾶Խ��ͬ�㣬���ˣ��˵����Խ�뾶ԽС����ͬ�㡢ͬ�˿����ӣ�����Խ��뾶Խ��ԭ�Ӱ뾶������K����3��Ԫ���Ƶ�����������ˮ���������Ԫ�ص�����������ˮ������ܷ�����Ӧ����4���¶�Խ�ߣ���Ԫ�ص��۳���Խ���Ȼ����۽��س�ʯ�����ȹ��̣���950��ʱ��������۳��ص����ʿ��Բ�ȡ�Ĵ�ʩ�dz�ֽ��裬���س�ʯ�۴�ɸ�С�Ŀ������������ĽӴ��������5��������������ԭ�����ɲ�ȡ���ط�������������˲����Ũ�ȣ�ƽ�������ƶ���
���㣺�������ʽ��д�����Ӱ뾶�ȽϺ�ƽ���ƶ�ԭ����

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�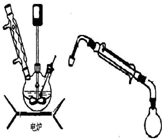 ˮ������Ϊһ����Ҫ�ľ�ϸ����ԭ�ϣ���ũҩ��ҽҩ���л��ϳ����й㷺��;�� �����ط��Ʊ�ˮ���£��ɷ�Ϊ�����Σ���һ��Ϊ�����Ȼ��Σ��ڶ���Ϊ����ˮ��Σ��ܷ�Ӧ����ʽΪ����NH2��2CO+NaClO+2NaOH��H2N-NH2?H2O+NaCl+Na2CO3��
ˮ������Ϊһ����Ҫ�ľ�ϸ����ԭ�ϣ���ũҩ��ҽҩ���л��ϳ����й㷺��;�� �����ط��Ʊ�ˮ���£��ɷ�Ϊ�����Σ���һ��Ϊ�����Ȼ��Σ��ڶ���Ϊ����ˮ��Σ��ܷ�Ӧ����ʽΪ����NH2��2CO+NaClO+2NaOH��H2N-NH2?H2O+NaCl+Na2CO3��