题目内容
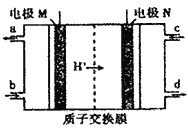
【题目】按下图装置进行实验,并回答下列问题
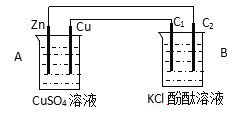
(1)判断装置的名称:A池为___________B池为____________
(2)铜极为______极,电极反应式为________________________,石墨棒C1为____极,电极反应式为___________________
【答案】 原电池 电解池 正 Cu2++2e-=Cu 阳极 2Cl--2e-=Cl2↑
【解析】(1)装置A中锌和铜以及硫酸铜溶液构成原电池,给装置B供电,因此装置B电解池;(2)锌的金属性强于铜,锌是负极,铜极为正极,电极反应式为Cu2++2e-=Cu;石墨棒C1与电源的正极相连,为阳极,发生氯离子失去电子的氧化反应,电极反应式为2Cl--2e-=Cl2↑。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
【题目】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) ![]() CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=________。
(2)该反应为________反应(填“吸热”或“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是(_____)
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为_____℃