题目内容
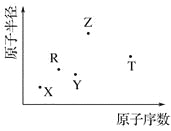
【题目】短周期主族元素 X、Y、Z、R、T 的原子半径与原子序数关系如下图所示。R 原子最外层电子数是电子层数的 2 倍,Y 与 Z 能形成 Z2Y、Z2Y2型离子化合物,Z 与 T 形成的化合物 Z2T 能破坏水的电离平衡。下列推断正确的是
A. 原子半径和离子半径均满足:Y<Z
B. 最高价氧化物对应水化物的酸性:T<R
C. 氢化物的沸点不一定是:Y>R
D. 由 X、R、Y、Z 四种元素组成的化合物水溶液一定显碱性
【答案】C
【解析】试题分析:X、Y、Z、R、T为五种短周期元素,根据图像可知X是H,R 原子最外层电子数是电子层数的 2 倍,R位于第二周期,则R是碳元素。Y 与 Z 能形成 Z2Y、Z2Y2型离子化合物,则Z是Na,Y是O。Z 与 T 形成的化合物 Z2T,能破坏水的电离平衡,所以T是S。A.氧离子半径大于钠离子半径,A错误;B.元素的非金属性越强,其最高价含氧酸的酸性越强,非金属性T>R,所以其最高价含氧酸酸性T>R,B错误;C.碳元素能形成多种氢化物,其沸点可能高于水,C正确;D.由 X、R、Y、Z 四种元素组成的化合物水溶液不一定显碱性,例如草酸氢钠,D错误;答案选C。

 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案【题目】T℃时。体积均为0.5L的两个恒容密闭容器中发生可逆反应:
2A(g)+B(g)![]() 2C(g)△H=-QkJ/mol(Q>0)
2C(g)△H=-QkJ/mol(Q>0)
实验测得反应在起始、达到平衡时的有关数据如下表:
容器编号 | 起始时各物质物质的量/mol | 达到平衡时体系能量的变化 | ||
A | B | C | ||
① | 2 | 1 | 0 | 0.75Q kJ |
② | 0.4 | 0.2 | 1.6 | |
下列叙述正确的是
A.容器①、②中反应的平衡常数均为36
B.容器②中反应达到平衡时放出的热量为0.05 Q kJ
C.向容器①中通入氦气,平衡时A的转化率不变
D.其他条件不变,若容器②保持恒容绝热,则达到平衡时C的体积分数小于2/3