题目内容
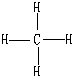
(1)某种粒子有1个原子核,核中有17个质子,20个中子,核外有18个电子,该粒子的化学符号是 .(2)某分子中有5个原子核,共有10个电子,这种分子的结构式是 .
(3)CaCl2是离子化合物,其电子式为: .
【答案】分析:(1)根据质子数确定原子序数,根据质子数与电子数的关系确定是否带电荷及电荷的多少、电性,根据质子数、中子数确定质量数;
(2)利用平均电子数判断元素,从而判断该分子的结构式;
(3)根据离子化合物电子式的书写规则写出电子式;
解答:解:(1)根据题意结合核内质子数=该元素的原子序数,确定该元素是氯元素,核内质子数比核外电子数少1,质量数=质子数+中子数,所以该微粒是带一个单位负电荷的质量数为37的阴离子,故答案为:1737Cl-
(2)5个原子核,共有10个电子,所以平均每个原子核有2个电子;因为原子的核外电子数=核内质子数=原子序数,所以必须有原子序数大于2的,有原子序数小于2的,小于2的只有H元素,所以该物质是甲烷,故答案为: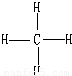
(3)氯化钙是离子化合物,形成的键是离子键,故答案为: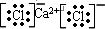 .
.
点评:电子式的书写,原子个数多的元素放中间,少的放周边;离子化合物中阴离子不能合并,复杂阳离子、阴离子书写时要用方括号括起来.
(2)利用平均电子数判断元素,从而判断该分子的结构式;
(3)根据离子化合物电子式的书写规则写出电子式;
解答:解:(1)根据题意结合核内质子数=该元素的原子序数,确定该元素是氯元素,核内质子数比核外电子数少1,质量数=质子数+中子数,所以该微粒是带一个单位负电荷的质量数为37的阴离子,故答案为:1737Cl-
(2)5个原子核,共有10个电子,所以平均每个原子核有2个电子;因为原子的核外电子数=核内质子数=原子序数,所以必须有原子序数大于2的,有原子序数小于2的,小于2的只有H元素,所以该物质是甲烷,故答案为:

(3)氯化钙是离子化合物,形成的键是离子键,故答案为:
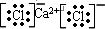 .
.点评:电子式的书写,原子个数多的元素放中间,少的放周边;离子化合物中阴离子不能合并,复杂阳离子、阴离子书写时要用方括号括起来.

练习册系列答案
相关题目