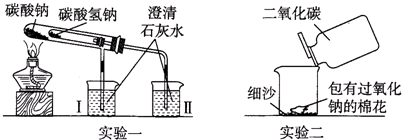
题目内容
下列叙述错误的是( )
| A.Na2CO3比NaHCO3稳定 |
| B.同一温度下,与等浓度的盐酸反应,生成CO2,NaHCO3比Na2CO3剧烈 |
| C.与同种酸反应生成等量的CO2时,所消耗的酸的量相等 |
| D.Na2CO3和NaHCO3都能与澄清石灰水反应得到白色沉淀 |
A.NaHCO3不稳定,加热易分解,而Na2CO3难以分解,故A正确;
B.Na2CO3与盐酸反应时分别发生Na2CO3+HCl=NaCl+NaHCO3(盐酸不足),Na2CO3+2HCl=2NaCl+H2O+CO2↑(盐酸过量),而NaHCO3+HCl=NaCl+H2O+CO2↑,故有NaHCO3与稀盐酸反应比Na2CO3与稀盐酸反应放出CO2剧烈,故B正确;
C.由反应Na2CO3+2HCl=2NaCl+H2O+CO2↑,NaHCO3+HCl=NaCl+H2O+CO2↑可知,等物质的量的Na2CO3和NaHCO3跟同一种盐酸充分反应生成等量的CO2时,消耗酸的量不等,故C错误;
D.碳酸钠和碳酸氢钠分别和氢氧化钙反应的方程式如下:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH NaHCO3+Ca(OH)2=CaCO3↓+H2O+NaOH,所以都能发生复分解反应生成沉淀,故D正确.
故选C.
B.Na2CO3与盐酸反应时分别发生Na2CO3+HCl=NaCl+NaHCO3(盐酸不足),Na2CO3+2HCl=2NaCl+H2O+CO2↑(盐酸过量),而NaHCO3+HCl=NaCl+H2O+CO2↑,故有NaHCO3与稀盐酸反应比Na2CO3与稀盐酸反应放出CO2剧烈,故B正确;
C.由反应Na2CO3+2HCl=2NaCl+H2O+CO2↑,NaHCO3+HCl=NaCl+H2O+CO2↑可知,等物质的量的Na2CO3和NaHCO3跟同一种盐酸充分反应生成等量的CO2时,消耗酸的量不等,故C错误;
D.碳酸钠和碳酸氢钠分别和氢氧化钙反应的方程式如下:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH NaHCO3+Ca(OH)2=CaCO3↓+H2O+NaOH,所以都能发生复分解反应生成沉淀,故D正确.
故选C.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目