题目内容
【题目】铜及其化合物在工业生产及生活中用途非常广泛。回答下列问题:
(1)基态铜原子价电子排布式为____________;第一电离能I(Cu)________I (Zn)(填“>”或“<”)
(2)配合物[Cu (CH3CN) 4] BF4[四氟硼酸四(乙腈)合铜(Ⅰ)]是有机合成中常见催化剂。
①该配合物中阴离子的空间构型为__________,与其互为等电子体的分子或离子是________(各举1例)。
②配体分子中与Cu(I) 形成配位键的原子为____________;配体CH3CN 中:碳原子杂化方式是______。
(3)已知Cu2O 熔点为1235 ℃,K2O 熔点为770℃,Cu2O 属于____晶体,前者熔点较高,其原因是______________________________________________________________________________
(4)Cu3N 的晶胞(立方)结构如下图所示:
①距离最近的两个Cu+间的距离为________nm。(保留两位小数)

②Cu3N 晶体的密度为____________ g·cm-3。(列出计算式,不必计算出结果)
【答案】 3d104s1 < 正四面体 CCl4 PO43- SO42- ClO4- N sp sp3 离子 Cu+离子半径比K+小,晶格能大 0.27 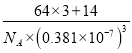 或
或![]()
【解析】试题分析:本题考查价电子排布式的书写、第一电离能大小的比较、空间构型的判断、等电子体的书写、晶体类型的判断和熔点高低的比较、晶胞的分析和计算。
(1)Cu的原子序数为29,Cu原子核外有29个电子,基态Cu原子的核外电子排布式为1s22s22p63s23p63d104s1,价电子排布式为3d104s1。Cu的价电子排布式为3d104s1,Zn的价电子排布式为3d104s2较稳定,所以第一电离能:I(Cu)![]() I(Zn)。
I(Zn)。
(2)①配合物中阴离子为BF4-,BF4-中中心原子B上的孤电子对数=![]() (3+1-4
(3+1-4![]() 1)=0,成键电子对数为4,价层电子对数为0+4=4,VSEPR模型为正四面体型,由于B上没有孤电子对,BF4-的空间构型为正四面体型。用替代法,与其互为等电子体的分子有CF4、CCl4、SiF4等,离子有SO42-、PO43-、ClO4-等。
1)=0,成键电子对数为4,价层电子对数为0+4=4,VSEPR模型为正四面体型,由于B上没有孤电子对,BF4-的空间构型为正四面体型。用替代法,与其互为等电子体的分子有CF4、CCl4、SiF4等,离子有SO42-、PO43-、ClO4-等。
②配体CH3CN中N上有孤电子对,与Cu(I)形成配位键的原子为N。配体CH3CN的结构式为 ,其中-CH3上C为sp3杂化,-CN上C为sp杂化。
,其中-CH3上C为sp3杂化,-CN上C为sp杂化。
(3)Cu2O的熔点较高,Cu2O属于离子晶体。Cu2O的熔点高于K2O的原因是:Cu2O和K2O都属于离子晶体,Cu+的离子半径小于K+的离子半径,Cu2O的晶格能大于K2O的晶格能,Cu2O的熔点高于K2O。
(4)用“均摊法”,晶胞中大白球的个数:8![]() =1个,小黑球:12
=1个,小黑球:12![]() =3,根据化学式Cu3N,大白球为N3-,小黑球为Cu+。
=3,根据化学式Cu3N,大白球为N3-,小黑球为Cu+。
①根据图示,距离最近的两个Cu+间的距离为![]() 0.381nm=0.27nm。
0.381nm=0.27nm。
②晶胞的体积为(0.381![]() 10-7)3cm3,1mol晶体的体积为NA
10-7)3cm3,1mol晶体的体积为NA![]() (0.381
(0.381![]() 10-7)3cm3=N
10-7)3cm3=N![]() 0.3813
0.3813![]() 10-21cm3,1mol晶体的质量为(3
10-21cm3,1mol晶体的质量为(3![]() 64+14)g=206g,Cu3N晶体的密度为
64+14)g=206g,Cu3N晶体的密度为![]() 1021g/cm3。
1021g/cm3。

 应用题作业本系列答案
应用题作业本系列答案


