题目内容
常温下,pH=12的氨水中存在以下电离平衡:
NH3·H2O NH4+ +OH-。往其中加入少量0.01 mol·L-1NaOH溶液,保持不变的是( )
NH4+ +OH-。往其中加入少量0.01 mol·L-1NaOH溶液,保持不变的是( )
| A.c(NH4+) | B.c(OH-) | C.c(NH3·H2O) | D.c(NH4+)·c(OH-) |
B
解析

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目
某pH=1的ZnCl2和HCl的混合溶液中含有FeCl3杂质,通过水解除去杂质,需将溶液调至pH=4,在调节溶液pH时,应选用的试剂是
| A.NaOH | B.ZnO | C.Na2CO3 | D.Fe2O3 |
下列有关结论中,正确的是
| A.浓度为0.lmol/LCuSO4溶液,温度升高,溶液的pH降低 |
| B.—元酸与—元碱恰好完全反应后的溶液中—定存在c(H+)=c(OH-) |
C.浓度相同的AlCl3、NH3 H2O、Ba(OH2)三物质的溶液,等体积混合时没有沉淀生成 H2O、Ba(OH2)三物质的溶液,等体积混合时没有沉淀生成 |
| D.在所有能够溶解Al(OH)3的溶液中Cu2+、ClO-、Cl-、 Ca2+一定能够大量共存 |
部分弱酸的电离平衡常数如下表:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡 常数(25℃) | Ki=1.77×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
下列选项正确的是( )。
A.2CN-+H2O+CO2=2HCN+CO32-
B.2HCOOH+CO32-=2HCOO-+H2O+CO2↑
C.等浓度的HCOONa和NaCN溶液的pH前者大于后者
D.中和等浓度的HCOOH和HCN消耗NaOH的量前者等于后者
25 ℃时,5种银盐的溶度积常数(Ksp)分别是:
| AgCl | Ag2SO4 | Ag2S | AgBr | AgI |
| 1.8×10-10 | 1.4×10-5 | 6.3×10-50 | 7.7×10-13 | 8.51×10-16 |
下列说法正确的是 ( )。
A.氯化银、溴化银和碘化银的溶解度依次增大
B.将硫酸银溶解于水后,向其中加入少量硫化钠溶液,不可能得到黑色沉淀
C.在5 mL 1.8×10-5 mol·L-1的NaCl溶液中,加入1滴(1 mL约20滴)0.1 mol·L-1的AgNO3溶液,不能观察到白色沉淀
D.将浅黄色溴化银固体浸泡在饱和氯化钠溶液中,可以有少量白色固体生成
下列叙述中,不正确的是 ( )。
| A.c(NH4+)相等的(NH4)2SO4和NH4Cl溶液中,溶质浓度大小关系:c[(NH4)2SO4]<c(NH4Cl) |
| B.向10 mL 0.10 mol·L-1的CH3COOH溶液中加入等物质的量的NaOH后,溶液中:c(Na+)=c(CH3COO-)>c(OH-)=c(H+) |
| C.两种不同浓度的HA溶液的物质的量浓度分别为c1和c2,pH分别为a和(a+1),则有c1≥10c2 |
| D.NaHCO3溶液中:c(H+)+c(H2CO3)=c(CO32—)+c(OH-) |
室温时,把10 mL pH=10的强碱溶液小心地加入到10 mL pH=4的某酸溶液中,在完全反应后的溶液中滴入紫色的石蕊试液时,溶液显红色,则此酸为( )
| A.一元强酸 | B.二元强酸 | C.任何强酸 | D.弱酸 |

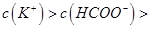

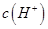

 ,且a=7.5
,且a=7.5
