题目内容
用惰性电极电解500mLNaCl溶液,当两极产生的气体总体积为16.8mL(标准状况)时,溶液的pH范围为
- A.8~10
- B.10~12
- C.5~6
- D.3~4
B
阳极:2Cl--2e-====Cl2↑;阴极:2H++2e-=====H2↑。
所以n(Cl2)=n(H2)= =3.75×10-4 mol
=3.75×10-4 mol
n(OH-)=2×3.75×10-4 mol=7.5×10-4 mol
c(OH-)=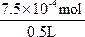 =1.5×10-3mol·L-1
=1.5×10-3mol·L-1
溶液中c(H+)=6.7×10-12 mol·L-1
pH=12-lg6.7
阳极:2Cl--2e-====Cl2↑;阴极:2H++2e-=====H2↑。
所以n(Cl2)=n(H2)=
 =3.75×10-4 mol
=3.75×10-4 moln(OH-)=2×3.75×10-4 mol=7.5×10-4 mol
c(OH-)=
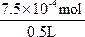 =1.5×10-3mol·L-1
=1.5×10-3mol·L-1溶液中c(H+)=6.7×10-12 mol·L-1
pH=12-lg6.7

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
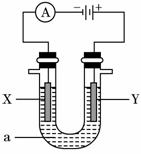 电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题: