题目内容
13.下列根据实验操作和现象所得出的结论正确的是( )| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向两份蛋白质溶液中分别滴加饱和NaCl 溶液和CuSO4 溶液 | 均有固体析出 | 蛋白质均发生变性 |
| B | 向溶液X 中先滴加稀硝酸,再滴加Ba(NO3)2溶液 | 出现白色沉淀 | 溶液X 中一定含有SO42- |
| C | 向一定浓度的Na2SiO3 溶液中通入适量CO2 气体 | 出现白色沉淀 | H2SiO3 的酸性比H2CO3的酸性强 |
| D | 处理锅炉水垢中的CaSO4时,依次加入饱和Na2CO3溶液和盐酸, | 水垢溶解 | Ksp:CaCO3<CaSO4 |
分析 A.滴加饱和NaCl发生盐析;
B.X中可能含亚硫酸根离子;
C.白色沉淀为硅酸,发生强酸制取弱酸的反应;
D.加入饱和Na2CO3溶液,发生沉淀的转化,碳酸钙可溶于盐酸.
解答 解:A.蛋白质溶于中滴加饱和NaCl发生盐析,而加CuSO4 溶液发生变性,故A错误;
B.白色沉淀为硫酸钡,X中可能含亚硫酸根离子或SO42-,亚硫酸根离子能被硝酸氧化,故B错误;
C.白色沉淀为硅酸,发生强酸制取弱酸的反应,则H2SiO3 的酸性比H2CO3的酸性弱,故C错误;
D.加入饱和Na2CO3溶液,发生沉淀的转化,则Ksp:CaCO3<CaSO4,碳酸钙可溶于盐酸,可处理水垢,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握有机物的结构与性质、离子的检验、酸性比较、沉淀的转化等为解答的关键,侧重分析与实验能力的考查,注意反应原理的应用,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.物质的浓度、体积都相同的NaF和NaCl溶液中,阴阳离子总数的大小关系正确的是( )
| A. | NaF=NaCl | B. | NaF>NaCl | C. | NaF<NaCl | D. | 无法确定 |
8.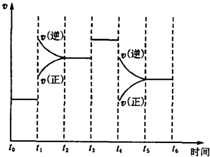 已知反应N2(g)+3H2(g)?2NH3(g),△H=-92.2kJ•mol-1.在某段时间t0~t6中反应速率与反应时间的曲线如图所示,则氨的平衡浓度最高的一段时间是( )
已知反应N2(g)+3H2(g)?2NH3(g),△H=-92.2kJ•mol-1.在某段时间t0~t6中反应速率与反应时间的曲线如图所示,则氨的平衡浓度最高的一段时间是( )
 已知反应N2(g)+3H2(g)?2NH3(g),△H=-92.2kJ•mol-1.在某段时间t0~t6中反应速率与反应时间的曲线如图所示,则氨的平衡浓度最高的一段时间是( )
已知反应N2(g)+3H2(g)?2NH3(g),△H=-92.2kJ•mol-1.在某段时间t0~t6中反应速率与反应时间的曲线如图所示,则氨的平衡浓度最高的一段时间是( )| A. | t2~t3 | B. | t0~t1 | C. | t4~t5 | D. | t6~t7 |
18.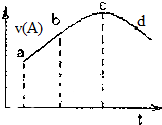 在恒温恒容的密闭容器中通入一定量的A、B,发生反应A(g)+2B(g)?3C(g)+D(l).如图是A的正反应速率v(A)随时间变化的示意图.下列说法正确的是( )
在恒温恒容的密闭容器中通入一定量的A、B,发生反应A(g)+2B(g)?3C(g)+D(l).如图是A的正反应速率v(A)随时间变化的示意图.下列说法正确的是( )
 在恒温恒容的密闭容器中通入一定量的A、B,发生反应A(g)+2B(g)?3C(g)+D(l).如图是A的正反应速率v(A)随时间变化的示意图.下列说法正确的是( )
在恒温恒容的密闭容器中通入一定量的A、B,发生反应A(g)+2B(g)?3C(g)+D(l).如图是A的正反应速率v(A)随时间变化的示意图.下列说法正确的是( )| A. | 反应物A的浓度:a点小于b点 | |
| B. | 可能是某种生物对反应起到的催化作用 | |
| C. | 曲线上的c、d两点都表示达到反应限度 | |
| D. | 平均反应速率:ab段大于bc段 |
5.下列说法正确的是( )
| A. | 判断共价化合物的依据:是否含有共价键 | |
| B. | 判断强弱电解质的依据:电解质溶解度大小 | |
| C. | 反应物和生成物所具有的总能量决定了该反应是放热还是吸热 | |
| D. | 在化学反应中,一定有化学键的断裂和形成,并伴有能量的变化 |
2.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | pH=1的溶液中:K+、Fe2+、MnO${\;}_{4}^{-}$、SO${\;}_{4}^{2-}$ | |
| B. | c(Fe3+)=0.1 mol•L-1的溶液中:K+、ClO-、SO${\;}_{4}^{2-}$、SCN- | |
| C. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的溶液中:NH${\;}_{4}^{+}$、Al3+、NO${\;}_{3}^{-}$、Cl- | |
| D. | 与铝反应生成氢气的溶液中:NH${\;}_{4}^{+}$、K+、Cl-、SiO${\;}_{3}^{2-}$ |
3.将m1 g的氢氧化钠和碳酸氢钠的固体混合物在300℃条件下充分加热,排出分解产生的气体,得到固体的质量为m2 g,设$\frac{{m}_{2}}{{m}_{1}}$=a,下列有关说法正确的是( )
| A. | a的取值范围是$\frac{53}{84}$<a<$\frac{53}{62}$ | |
| B. | a=$\frac{53}{65}$,固体成分为碳酸钠和氢氧化钠 | |
| C. | a=$\frac{53}{75}$时,固体成分为碳酸钠 | |
| D. | 加热过程中产生二氧化碳的物质的量总是小于水的物质的量 |
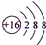 ,B
,B ,C
,C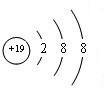 ,D
,D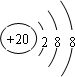 .它们离子的半径由大到小的顺序是r(S2-)>r(Cl-)>r(K+)>r(Ca2+).
.它们离子的半径由大到小的顺序是r(S2-)>r(Cl-)>r(K+)>r(Ca2+). 金刚烷、立方烷的合成在有机合成史上具有理论意义.
金刚烷、立方烷的合成在有机合成史上具有理论意义.