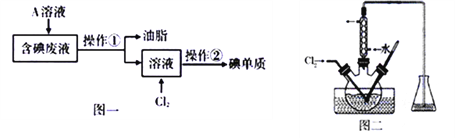
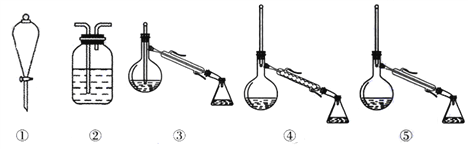
题目内容
【题目】有机化合物甲和G都在生活中有很多用途,其合成路线如下:

已知:①R1—CHO+R2—CH2—CHO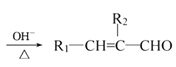 (R1、R2代表烃基或氢原子)
(R1、R2代表烃基或氢原子)
②D与A互为同系物;在相同条件下,D蒸气相对于氢气的密度为39。
(1)A的分子式是____,G中含氧官能团的名称是____。
(2)②的反应类型是____, F的结构简式为______。
(3)B的核磁共振氢谱有____组峰,峰面积之比为_____________。
(4)C有多种同分异构体,其中属于芳香族化合物的有____种。
(5)写出反应①的化学方程式:_____________。
(6)设计实验检验E中的官能团(说明实验操作步骤、现象及结论)____________
(7)G的同分异构体 是一种重要的药物中间体,其合成路线与G相似,请以
是一种重要的药物中间体,其合成路线与G相似,请以![]() 为原料设计它的合成路线(其他所需原料自选,注明反应条件)________。
为原料设计它的合成路线(其他所需原料自选,注明反应条件)________。
【答案】 C7H8 羧基 加成反应 ![]() 4组峰 2:2:2:1 4
4组峰 2:2:2:1 4 ![]() +CH3COOH
+CH3COOH![]()
![]() +H2O 取适量E溶液于试管中,先加入过量的新制的氢氧化铜悬浊液,加热煮沸,出现砖红色的沉淀,证明含醛基;酸化后,再加溴水或酸性高锰酸钾溶液,溶液褪色,则证明含碳碳双键
+H2O 取适量E溶液于试管中,先加入过量的新制的氢氧化铜悬浊液,加热煮沸,出现砖红色的沉淀,证明含醛基;酸化后,再加溴水或酸性高锰酸钾溶液,溶液褪色,则证明含碳碳双键 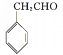
![]()
![]()
![]()
![]()
【解析】D与A互为同系物;在相同条件下,D蒸气相对于氢气的密度为39,则相对分子质量为78,结合Cl3CCHO与D反应生成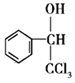 可推出D为苯,A为苯的同系物,且经过多步反应生成苯甲醛,故A为甲苯,甲苯在光照条件下与氯气发生取代反应生成B为
可推出D为苯,A为苯的同系物,且经过多步反应生成苯甲醛,故A为甲苯,甲苯在光照条件下与氯气发生取代反应生成B为![]() ,
,![]() 在氢氧化钠的水溶液中加热发生取代反应生成C为
在氢氧化钠的水溶液中加热发生取代反应生成C为![]() ,
,![]() 在铜的催化下发生氧化反应生成
在铜的催化下发生氧化反应生成![]() ,
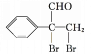
,![]() 与乙醛在稀氢氧化钠溶液中加热发生加成反应得到E为
与乙醛在稀氢氧化钠溶液中加热发生加成反应得到E为![]() ,
,![]() 与溴的四氯化碳溶液发生加成反应生成F为
与溴的四氯化碳溶液发生加成反应生成F为![]() ,
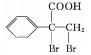
,![]() 在催化剂作用下与氧气发生氧化反应生成G为
在催化剂作用下与氧气发生氧化反应生成G为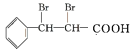 。(1)A为甲苯,分子式是C7H8,G为
。(1)A为甲苯,分子式是C7H8,G为 ,含氧官能团的名称是羧基;(2)②是
,含氧官能团的名称是羧基;(2)②是![]() 与三氯甲烷在碱溶液中发生加成反应生成
与三氯甲烷在碱溶液中发生加成反应生成 ,反应类型是加成反应, F的结构简式为
,反应类型是加成反应, F的结构简式为![]() ;(3)B为
;(3)B为![]() ,的核磁共振氢谱有4组峰,峰面积之比为2:2:2:1;(4)C为
,的核磁共振氢谱有4组峰,峰面积之比为2:2:2:1;(4)C为![]() ,有多种同分异构体,其中属于芳香族化合物的有甲苯醚、对甲基苯酚、间甲基苯酚、邻甲基苯酚共4种;(5)反应①是
,有多种同分异构体,其中属于芳香族化合物的有甲苯醚、对甲基苯酚、间甲基苯酚、邻甲基苯酚共4种;(5)反应①是 与乙酸发生酯化反应生成
与乙酸发生酯化反应生成![]() ,反应的化学方程式为:
,反应的化学方程式为: ![]() +CH3COOH
+CH3COOH![]()
![]() +H2O;(6)E为
+H2O;(6)E为![]() ,所含官能团为碳碳双键和醛基,必须先检验醛基再检验碳碳双键,故检验方法为:取适量E溶液于试管中,先加入过量的新制的氢氧化铜悬浊液,加热煮沸,出现砖红色的沉淀,证明含醛基;酸化后,再加溴水或酸性高锰酸钾溶液,溶液褪色,则证明含碳碳双键;(7)G的同分异构体
,所含官能团为碳碳双键和醛基,必须先检验醛基再检验碳碳双键,故检验方法为:取适量E溶液于试管中,先加入过量的新制的氢氧化铜悬浊液,加热煮沸,出现砖红色的沉淀,证明含醛基;酸化后,再加溴水或酸性高锰酸钾溶液,溶液褪色,则证明含碳碳双键;(7)G的同分异构体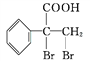 是一种重要的药物中间体,其合成路线与G相似,
是一种重要的药物中间体,其合成路线与G相似, ![]() 与甲醛在稀氢氧化钠溶液中加热反应生成
与甲醛在稀氢氧化钠溶液中加热反应生成![]() ,
,![]() 与溴的四氯化碳溶液反应生成
与溴的四氯化碳溶液反应生成 ,
, 催化氧化得到
催化氧化得到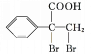 ,合成路线如下:
,合成路线如下: 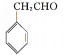
![]()
![]()
![]()

![]()

。

 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案【题目】某蓄电池反应为NiO2+Fe+2H2O![]() Fe(OH)2+Ni(OH)2。
Fe(OH)2+Ni(OH)2。
(1)该蓄电池充电时,发生还原反应的物质是 (填下列字母),放电时生成Fe(OH)2的质量18 g,则外电路中转移的电子数是 。
A.NiO2 B.Fe C.Fe(OH)2 D.Ni(OH)2
(2)为防止远洋轮船的钢铁船体在海水中发生电化学腐蚀,通常把船体与浸在海水里的Zn块相连,或与该蓄电池这样的直流电源的 极(填“正”或“负”)相连。
(3)以该蓄电池做电源,用右图所示装置,在实验室模拟铝制品表面“钝化”处理的过程中,发现溶液逐渐变浑浊,原因是(用相关的电极反应式和离子方程式表示)。 。

(4)精炼铜时,粗铜应与直流电源的 极(填“正”或“负”)相连,精炼过程中,电解质溶液中c(Fe2+)、c(Zn2+)会逐渐增大而影响进一步电解,甲同学设计如下除杂方案:
![]()
已知:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
开始沉淀时的pH | 2.3 | 7.5 | 5.6 | 6.2 |
完全沉淀时的pH | 3.9 | 9.7 | 6.4 | 8.0 |
则加入H2O2的目的是 ,乙同学认为应将方案中的pH调节到8,你认为此观点 (填“正确”或“不正确”),理由是 。
【题目】已知反应A(g)+B(g) ![]() C(g)+D(g)的平衡常数K值与温度的关系如表所示,830 ℃时,向一个2 L的密闭容器中充入0.20 mol A和0.20 mol B,10 s时达平衡。下列说法不正确的是
C(g)+D(g)的平衡常数K值与温度的关系如表所示,830 ℃时,向一个2 L的密闭容器中充入0.20 mol A和0.20 mol B,10 s时达平衡。下列说法不正确的是
温度/℃ | 700 | 830 | 1200 |
K值 | 1.7 | 1.0 | 0.4 |
A. 达到平衡后,B的转化率为50%
B. 增大压强,正、逆反应速率均加快
C. 该反应为吸热反应,升高温度,平衡正向移动
D. 反应初始至平衡,A的平均反应速率v(A)=0.005 mol·L-1·s-1