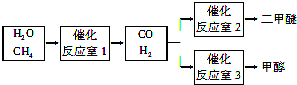
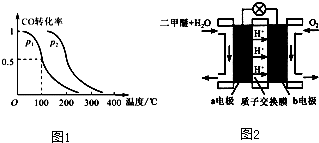
��Ŀ����
CO��g��+H2O��g��?CO2��g��+H2��g��+Q����1mol CO��1mol H2O�����ܱ������з���������Ӧ�������������������£�����������ȷ���ǣ�������
������A�������ı䷴Ӧ���ʣ����ı仯ѧƽ�⣬��Ӧ�ų����������䣻
B����Ӧ�������������ķ�Ӧ������ѹǿ��ƽ�ⲻ�䣬��Ӧ���Ȳ��䣻
C�����·�Ӧ���ʼӿ죬ƽ�������ȷ�Ӧ������У���Ӧ���ȷ����仯��
D�����Ѹ÷�Ӧ��Ƴ�ԭ��أ���ѧ�ܳ�ת���������⣬��ת���ɵ��ܣ����Էų�������Ӧ���٣�
B����Ӧ�������������ķ�Ӧ������ѹǿ��ƽ�ⲻ�䣬��Ӧ���Ȳ��䣻
C�����·�Ӧ���ʼӿ죬ƽ�������ȷ�Ӧ������У���Ӧ���ȷ����仯��
D�����Ѹ÷�Ӧ��Ƴ�ԭ��أ���ѧ�ܳ�ת���������⣬��ת���ɵ��ܣ����Էų�������Ӧ���٣�
����⣺A�������ı䷴Ӧ���ʣ��ı䷴Ӧ;�����ı仯ѧƽ�⣬��Ӧ�ų����������䣬��A����
B����Ӧ�������������ķ�Ӧ������ѹǿ����ѧƽ�ⲻ�����ƶ�����Ӧ���Ȳ��䣬��B��ȷ��
C�����·�Ӧ���ʼӿ죬ƽ�������ȷ�Ӧ������У���Ӧ����һ�������仯����C����
D�����Ѹ÷�Ӧ��Ƴ�ԭ��أ���ѧ�ܳ�ת���������⣬��ת���ɵ��ܣ����Էų�������Ӧ���٣���D����
��ѡB��
B����Ӧ�������������ķ�Ӧ������ѹǿ����ѧƽ�ⲻ�����ƶ�����Ӧ���Ȳ��䣬��B��ȷ��
C�����·�Ӧ���ʼӿ죬ƽ�������ȷ�Ӧ������У���Ӧ����һ�������仯����C����
D�����Ѹ÷�Ӧ��Ƴ�ԭ��أ���ѧ�ܳ�ת���������⣬��ת���ɵ��ܣ����Էų�������Ӧ���٣���D����
��ѡB��
���������⿼���˻�ѧƽ���ƶ�ԭ�������жϣ���Ӧ�����仯��ƽ���ƶ��ķ���Ӧ�ã����ջ����ǹؼ�����Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
��֪����CO��g��+
O2��g���TCO2��g����H=-283.0kJ?mol-1��H2��g��+
O2��g���TH2O��g����H=-241.8kJ?mol-1����CO��g��+H2O��g���TH2��g��+CO2��g���ġ�HΪ��������
| 1 |
| 2 |
| 1 |
| 2 |
| A��+41.2 kJ?mol-1 |
| B��-41.2 kJ?mol-1 |
| C��+82.4kJ?mol-1 |
| D��-524.8 kJ?mol-1 |
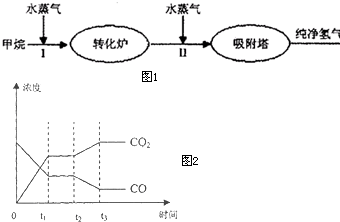 ����Bay�ȹ���ʹ��ʯ�����ѽ�ĸ������������ȡ������������������ͼ1��
����Bay�ȹ���ʹ��ʯ�����ѽ�ĸ������������ȡ������������������ͼ1��