题目内容
某元素一种同位素的原子的质子数为m,中子数为n,则下列说法正确的是( )
A.这种元素的相对原子质量为(m+n)
B.若碳原子质量为Wg此原子的质量为(m+n)W g
C.不能由此确定该元素的相对原子质量
D.核内中子的总质量小于质子的总质量
【答案】
C
【解析】
试题分析:因质子数+中子数求得的是原子的质量数,元素存在同位素,所以该元素的质量数不是(m+n),故A错误;该元素的相对原子质量等于各核素的相对原子质量乘以同位素的原子百分数算出来的平均值,所以不能由此确定该元素的相对原子质量,则选项C正确,BD是错误的,答案选C。
考点:考查同位素以及元素相对原子质量的计算
点评:该题是高考中的常见考点,属于中等难度的试题,试题综合性强,旨在培养学生灵活运用基础知识解决实际问题的能力。本题在判断时注意掌握核素的元素相对原子质量的求法,注意与质量数的区别。

练习册系列答案
相关题目
 ,用X射线研究其固体表明,在边长为1.00×
,用X射线研究其固体表明,在边长为1.00× 的立方体中含有20个原子.R在化学反应中常表现为+2价、+4价.在溶液中
的立方体中含有20个原子.R在化学反应中常表现为+2价、+4价.在溶液中 稳定,而
稳定,而 有强氧化性,可将NO氧化为
有强氧化性,可将NO氧化为 .氧化物
.氧化物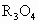 ,其性质与
,其性质与 有些类似.R的另一种质量数比R少2的同位素较为稳定,与铁可形成合金,在潮湿环境中易形成铁锈.R的单质及化合物在工农业生产、医疗卫生、科学技术等各个领域都有很多用途.
有些类似.R的另一种质量数比R少2的同位素较为稳定,与铁可形成合金,在潮湿环境中易形成铁锈.R的单质及化合物在工农业生产、医疗卫生、科学技术等各个领域都有很多用途. 溶液中,是否会发生反应?
溶液中,是否会发生反应? 反应,生成R的氧化物、R的硝酸盐和水三种物质,此反应的方程式为________.
反应,生成R的氧化物、R的硝酸盐和水三种物质,此反应的方程式为________.