题目内容
【题目】Ⅰ.掌握仪器的名称、组装及使用方法是中学化学实验的基础,观察下图实验装置。
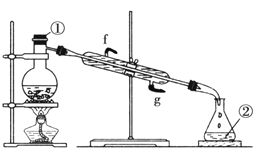
(1)写出图中玻璃仪器的名称:①______________,②______________。
(2)若利用该装置分离四氯化碳和酒精的混合物,还缺少的仪器有___________。
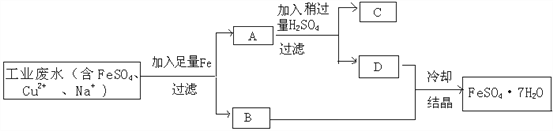
Ⅱ.柠檬酸亚铁(FeC6H6O7)是一种易吸收的高效铁制剂,可由绿矾(FeSO47H2O)通过下列反应制备:FeSO4+Na2CO3 = FeCO3↓+Na2SO4 FeCO3+C6H8O7 = FeC6H6O7+CO2↑+H2O。
(1)生成的FeCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是_____________。
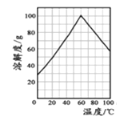
(2)结合如图绿矾溶解度曲线,要从FeSO4溶液中得到FeSO47H2O晶体,先通过____得到_____℃饱和溶液,再冷却至_____℃结晶,过滤,少量冰水洗涤,低温干燥。
【答案】 蒸馏烧瓶 锥形瓶 温度计 取最后一次洗涤液于试管中,加入盐酸酸化的BaCl2溶液,若无白色沉淀生成,则洗涤完全,反之则未洗涤完全 蒸发浓缩 60 0
【解析】Ⅰ.(1)根据仪器构造判断仪器名称。
(2)根据四氯化碳和酒精的沸点相差较大,需要蒸馏分离判断。
Ⅱ.(1)根据碳酸亚铁表面有吸附的硫酸根离子分析。
(2)根据硫酸亚铁的溶解度随温度的升高先增大后减小分析。
Ⅰ、(1)根据仪器的构造可判断图中玻璃仪器的名称为①是蒸馏烧瓶,②是锥形瓶。(2)若利用该装置分离四氯化碳和酒精的混合物,由于二者互溶,沸点相差较大,所以需要蒸馏,因此需要控制温度,还缺少的仪器有温度计。
Ⅱ、(1)硫酸亚铁参与反应,生成的FeCO3沉淀表面有吸附的硫酸根离子,所以检验洗涤是否完全的方法是通过检验硫酸根离子实现,即取最后一次洗涤液于试管中,加入盐酸酸化的BaCl2溶液,若无白色沉淀生成,则洗涤完全,反之则未洗涤完全。
(2)根据绿矾溶解度曲线可知随着温度的升高溶解度增大,但增大到一定程度后开始降低,因此要从FeSO4溶液中得到FeSO47H2O晶体,先通过蒸发浓缩得到60℃饱和溶液,再冷却至0℃结晶,过滤,少量冰水洗涤,低温干燥即可。

 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案