题目内容
下列离子方程式中,正确的是( )
A.氯气通入水中,溶液呈酸性:Cl2+H2O  2H++Cl-+ClO- 2H++Cl-+ClO- |
B.用铜做电极电解CuSO4溶液:2Cu2++2H2O 2Cu +O2↑+4H+ 2Cu +O2↑+4H+ |
C.NaHS电离方程式:NaHS  Na++HS- Na++HS- |
D.NH4Cl水解反应:NH4++2H2O  NH3·H2O+H3O+ NH3·H2O+H3O+ |
D
解析试题分析:A、氯气通入水中与水反应生成盐酸和次氯酸,HClO为弱电解质,应该用化学式,错误;B、用铜做电极电解CuSO4溶液,铜是活泼电极,阳极反应为:Cu - 2e-=Cu2+,而不是OH-放电,错误;C、NaHS属于盐类为强电解质,连接符号应该用等号,错误;D、NH4Cl水解反应:NH4++2H2O  NH3·H2O+H3O+,正确。
NH3·H2O+H3O+,正确。
考点:考查离子方程式正误判断。

练习册系列答案
相关题目
甲、乙、丙、丁是由H+、Na+、Al3+、Ba2+、OH—、Cl—、HCO3—离子中的两种组成,可以发生如图转化,下列说法正确的是
| A.甲为AlCl3,乙为NaHCO3 |
| B.溶液丙中还可以大量共存的离子有:Fe2+、NO3—、SO42— |
| C.在甲中滴加丁开始反应的离子方程式:HCO3—+ Ba2++OH—= BaCO3↓+ H2O。 |
| D.白色沉淀A可能溶解在溶液D中。 |
下列两种物质的溶液混合后不能发生离子反应的是( )
| A.HNO3和Na2CO3 | B.NaCl和AgNO3 |
| C.K2SO4和BaCl2 | D.HNO3和BaCl2 |
下列关于电解质、非电解质的说法正确的是
| A.氯气溶于水得氯水,该溶液能导电,因此氯气是电解质 |
| B.CaCO3饱和溶液导电能力很弱,故CaCO3是弱电解质 |
| C.导电能力弱的溶液肯定是弱电解质的溶液 |
| D.HF的水溶液中既有H+、F-,又有大量的HF分子,因此HF是弱电解质 |
下列叙述正确的是( )
| A.液态HCl不导电,所以HCl是非电解质 |
| B.NH3的水溶液能够导电,所以NH3是电解质 |
| C.液态Cl2不导电,所以Cl2是非电解质 |
| D.BaSO4在熔融状态下能导电,所以BaSO4是电解质 |
能正确表示下列反应的离子方程式是( )
A.向次氯酸钙溶液通入过量CO2: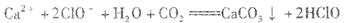 |
B.向次氯酸钙溶液通入SO2: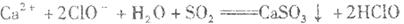 |
C.氢氧化钙溶液与碳酸氢镁溶液反应: |
D.氯化亚铁溶液中加入稀硝酸: |
在下列给定条件的溶液中,一定能大量共存的离子组是
| A.无色溶液:Ca2+、H+、Cl-、HSO3- |
| B.能使pH试纸呈红色的溶液:Na+、Fe2+、Cl-、NO3- |
| C.Na2CO3溶液:K+、Fe3+、NO3-、NO3- |
D.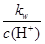 =0.1 mol/L的溶液:Na+、K+、SiO32-、NO3- =0.1 mol/L的溶液:Na+、K+、SiO32-、NO3- |
下列物质水溶液能导电,但该物质属于非电解质的是
| A.Na2O | B.Cl2 | C.H2SO4 | D.SO2 |
