题目内容
做实验时不小心使皮肤上粘了一些高锰酸钾,形成的黑斑很久才能消除,如果用草酸(乙二酸)的稀溶液洗涤,黑斑可以迅速退去,其离子方程式为:MnO4-+H2C2O4+H+→CO2↑+Mn2++.下列有关叙述正确的是
- A.发生还原反应的是H2C2O4
- B.该离子方程式右侧方框内的产物是OH-
- C.1 mol草酸分子中含9mol共用电子对
- D.10 mol H+参加反应时,电子转移5mol
C
分析:A、化合价降低的元素所在反应物是氧化剂被还原发生还原反应;
B、根据原子守恒、电子守恒和电荷守恒来配平离子方程式;
C、依据草酸的分子结构分析计算;
D、根据原子守恒、电子守恒和电荷守恒来配平离子方程式,结合反应的定量关系计算电子转移.
解答:A、化合价降低的元素是锰元素,所在反应物KMnO4是氧化剂被还原发生还原反应,H2C2O4中碳元素化合价升高做还原剂被氧化发生氧化反应,故A错误;
B、根据电子守恒,该反应中锰元素化合价降低5价,两碳元素化合价共升高2价,所以反应转移电子数为10,所以可以得到:2MnO4-+5H2C2O4+H+→10CO2↑+2Mn2++□,根据电荷守恒、原子守恒,所以□中为8H2O,H+的计量数是6,故B错误;
C、草酸的分子结构式两个羧基连接形成的化合物为HOOC-COOH,分子中形成的共价键共9个,1 mol草酸分子中含9mol共用电子对 故C正确;
D、根据原子守恒、电子守恒和电荷守恒来配平离子方程式为:2MnO4-+5H2C2O4+6H+═10CO2↑+2Mn2++8H2O,6H+~10mle-,所以10 mol H+参加反应时,电子转移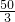 mol,故D正错误;
mol,故D正错误;
故选C.
点评:本题考查学生氧化还原反应中的综合知识,主要是氧化还原反应的配平应用,要求学生具有分析和解决问题的能力,难度较大.
分析:A、化合价降低的元素所在反应物是氧化剂被还原发生还原反应;
B、根据原子守恒、电子守恒和电荷守恒来配平离子方程式;
C、依据草酸的分子结构分析计算;
D、根据原子守恒、电子守恒和电荷守恒来配平离子方程式,结合反应的定量关系计算电子转移.
解答:A、化合价降低的元素是锰元素,所在反应物KMnO4是氧化剂被还原发生还原反应,H2C2O4中碳元素化合价升高做还原剂被氧化发生氧化反应,故A错误;
B、根据电子守恒,该反应中锰元素化合价降低5价,两碳元素化合价共升高2价,所以反应转移电子数为10,所以可以得到:2MnO4-+5H2C2O4+H+→10CO2↑+2Mn2++□,根据电荷守恒、原子守恒,所以□中为8H2O,H+的计量数是6,故B错误;
C、草酸的分子结构式两个羧基连接形成的化合物为HOOC-COOH,分子中形成的共价键共9个,1 mol草酸分子中含9mol共用电子对 故C正确;
D、根据原子守恒、电子守恒和电荷守恒来配平离子方程式为:2MnO4-+5H2C2O4+6H+═10CO2↑+2Mn2++8H2O,6H+~10mle-,所以10 mol H+参加反应时,电子转移
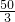 mol,故D正错误;
mol,故D正错误;故选C.
点评:本题考查学生氧化还原反应中的综合知识,主要是氧化还原反应的配平应用,要求学生具有分析和解决问题的能力,难度较大.

练习册系列答案
相关题目
做实验时不小心使皮肤上粘了一些高锰酸钾,形成的黑斑很久才能消除,如果用乙二酸的稀溶液洗涤,黑斑可以迅速褪去,其离子方程式为MnO4—+H2C2O4+H+→CO2↑+Mn2++ 。下列有关叙述正确的是( )
| A.发生还原反应的是H2C2O4 | B.该离子方程式右侧方框内的产物是OH— |
| C.10mol CO2生成时,电子转移5 mol | D.1 mol乙二酸分子中含有7molσ键 |
 .下列有关叙述正确的是( )
.下列有关叙述正确的是( )