题目内容
8.下列说法错误的是( )| A. | 分类方法应用广泛 | |
| B. | 纳米级粒子与胶体粒子的尺寸大致相当 | |
| C. | 胶体属于介稳体系 | |
| D. | 区分胶体与溶液的方法必须用丁达尔现象 |
分析 A.分类是研究的一种重要方法;
B.纳米级粒子微粒直径大小在1--100纳米之间;
C.胶体比较稳定;
D.胶体有而溶液没有的性质可用于区分溶液和胶体,不止丁达尔效应.
解答 解:A.分类是研究的一种重要方法,应用广泛,故A正确;
B.纳米级粒子和胶体的微粒直径大小在1--100纳米之间,故B正确;
C.胶体比较稳定,属于介稳体系,故C正确;
D.胶体有而溶液没有的性质可用于区分溶液和胶体,如有:①丁达尔现象;②电泳;③聚沉(受热法、加入电解质法、加入带相反电荷的另一种胶体法)等,故D错误.
故选D.
点评 本题考查胶体的性质,难度不大,注意基础知识的掌握,D选项为易错点.

练习册系列答案
相关题目
18.下列离子方程式中,正确的是( )
| A. | 稀硫酸与氢氧化钡溶液反应:H++OH-═H2O | |
| B. | 铁与氯化铁溶液反应:Fe+2Fe3+═3Fe2+ | |
| C. | 实验室制氯气:MnO2+4HCl═Mn2++2Cl-+Cl2↑+2H2O | |
| D. | 向氯化铝溶液滴加少量氨水:Al3++3OH-═Al(OH)3↓ |
16.NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 常温常压下,2g 氢气所含原子数目为2NA | |
| B. | 36g H2O中含有的质子数为10NA | |
| C. | 标准状况下,11.2L水中含有的分子数是0.5NA | |
| D. | 1mol 氯气与足量水反应,转移的电子数是2NA |
3.相同温度下,下列物质中导电能力最强的是( )
| A. | 100mL 0.1mol/L 的KOH溶液 | B. | 2L 0.1mol/L的CH3COOH溶液 | ||
| C. | 100mL 0.1mol/L的HF溶液 | D. | 100mL0.1mol/L的K2SO4溶液 |
13.已知:乙酸乙酯(C4H8O2)通常是无色液体,不溶于饱和碳酸钠溶液,密度小于1g•mL-1,要从饱和碳酸钠溶液与乙酸乙酯的混合物里将乙酸乙酯分离出来,试判断下列分离方法中最合理的是( )
| A. | 蒸馏 | B. | 分液 | C. | 过滤 | D. | 蒸发 |
20.下列关于强弱电解质的说法,错误的是( )
| A. | 强电解质在溶液中完全电离,不存在电离平衡 | |
| B. | 纯净的强电解质在液态时,有的导电,有的不导电 | |
| C. | 同一弱电解质的溶液,当温度、浓度不同时,其导电能力也不同 | |
| D. | 在溶液中,导电能力强的电解质为强电解质,导电能力弱的电解质是弱电解质 |
 ;
;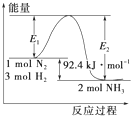 是可逆反应反应物不能完全转化.
是可逆反应反应物不能完全转化.