题目内容
下列结论正确的是( )
①微粒半径:Fe(OH)3胶粒>S2->Cl>S>F ②氢化物稳定性:HF>HCl>H2S>H2Se
③离子还原性:Fe3+>Cu2+>Fe2+>Zn2+ ④单质氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>HClO4>H2SeO4 ⑥熔沸点:Na>H2O>HF>HCl.
①微粒半径:Fe(OH)3胶粒>S2->Cl>S>F ②氢化物稳定性:HF>HCl>H2S>H2Se
③离子还原性:Fe3+>Cu2+>Fe2+>Zn2+ ④单质氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>HClO4>H2SeO4 ⑥熔沸点:Na>H2O>HF>HCl.
| A.①②④ | B.②④⑥ | C.只有① | D.只有⑥ |
①胶体的粒子半径大于离子和原子,电子层越多,半径越大,同周期从左向右原子半径在减小,则Fe(OH)3胶粒>
S2->S>Cl>F,故①错误;
②非金属性越强,气态氢化物越稳定,非金属性F>Cl>S>Se,则氢化物稳定性为HF>HCl>H2S>H2Se,故②正确;
③金属性越强,对应离子的氧化性越弱,金属性Zn>Fe>Cu,则离子氧化性为Fe3+>Cu2+>Fe2+>Zn2+,故③错误;
④非金属性越强,对应单质的氧化性越强,非金属性Cl>S>Se>Te,单质氧化性:Cl2>S>Se>Te,故④正确;
⑤非金属性越强,对应的最高价含氧酸的酸性越强,非金属性Cl>S>Se,则酸性为HClO4>H2SO4>H2SeO4,故⑤错误;
⑥金属晶体的熔沸点大于分子晶体的,但分子晶体中含有氢键的沸点反常的高,则熔沸点:Na>H2O>HF>HCl,故⑥正确;
故选B.
S2->S>Cl>F,故①错误;
②非金属性越强,气态氢化物越稳定,非金属性F>Cl>S>Se,则氢化物稳定性为HF>HCl>H2S>H2Se,故②正确;
③金属性越强,对应离子的氧化性越弱,金属性Zn>Fe>Cu,则离子氧化性为Fe3+>Cu2+>Fe2+>Zn2+,故③错误;
④非金属性越强,对应单质的氧化性越强,非金属性Cl>S>Se>Te,单质氧化性:Cl2>S>Se>Te,故④正确;
⑤非金属性越强,对应的最高价含氧酸的酸性越强,非金属性Cl>S>Se,则酸性为HClO4>H2SO4>H2SeO4,故⑤错误;
⑥金属晶体的熔沸点大于分子晶体的,但分子晶体中含有氢键的沸点反常的高,则熔沸点:Na>H2O>HF>HCl,故⑥正确;
故选B.

练习册系列答案
相关题目
己知:2C(s)+O2(g)═2CO(g)△H=-221.0kJ?mol-1
2CO(g)+O2(g)═2CO2(g)△H=-566.0kJ?mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1
下列结论正确的是( )
2CO(g)+O2(g)═2CO2(g)△H=-566.0kJ?mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1
下列结论正确的是( )
| A、H2的燃烧热△H=-241.8kJ?mol-1 | B、炭和和水蒸气转化为水煤气为放热反应 | C、将24g 炭完全转化为水煤气,再充分燃烧,整个过程反应热为-787.0kJ?mol-1 | D、1mol H2O(g)完全分解需要吸收241.8kJ热量 |
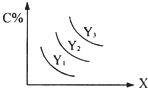 对于反应A(s)+2B(g?3C(g);△H>0,C%跟外界条件X、Y的关系如图所示,下列结论正确的是( )
对于反应A(s)+2B(g?3C(g);△H>0,C%跟外界条件X、Y的关系如图所示,下列结论正确的是( )| A、Y表示温度,X表示压强,且Y3>Y2>Y1 | B、Y表示压强,X表示温度,且Y3>Y2>Y1 | C、X表示压强,Y表示温度,且Y1>Y2>Y3 | D、X表示温度,Y表示压强,且Y1>Y2>Y3 |