题目内容
某固体混合物可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的一种或几种组成,现对该混合物做如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积):
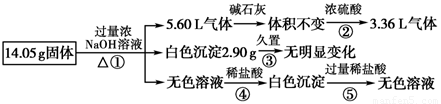
下列说法正确的是
A.固体混合物中一定含有Al,但质量不可确定
B.固体混合物中可能含有MgCl2和AlCl3
C.固体混合物中一定含有MgCl2和FeCl2
D.固体混合物中一定含有 (NH4)2SO4、MgCl2
【答案】
D
【解析】
试题分析:加入过量NaOH溶液,生成5.60L气体,通入浓硫酸变为3.36L,说明生成了H23.36L,物质的量为0.15mol,NH3为2.24L,物质的量为0.1mol,则原固体含(NH4)2SO4 0.05mol,质量为6.60g,含Al 0.1mol,质量为2.70g;产生的白色沉淀久置无明显变化,说明不是Fe(OH)2,原化合物不含FeCl2,故2.90g白色沉淀全部是Mg(OH)2,则MgCl2的质量为4.75g,2.70g Al、6.60g (NH4)2SO4,4.75g MgCl2的质量和正好为14.05g,所以原混合物一定不含AlCl3,故D项正确。
考点:本题考查物质的推断。

练习册系列答案
相关题目
某固体混合物可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的一种或几种组成,现对该混合物做如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积):

下列说法正确的是( )

下列说法正确的是( )
| A、固体混合物中一定含有Al,但质量不可确定 | B、固体混合物中可能含有MgCl2和AlCl3 | C、固体混合物中一定含有MgCl2和FeCl2 | D、固体混合物中一定含有(NH4)2SO4、MgCl2 |