题目内容
18.化学与人类生产、生活环境密切相关.下列说法正确的是( )| A. | 石油分馏、煤的气化、煤的干馏、海水制盐等都属于化学变化过程 | |
| B. | 水泥、玻璃、陶瓷是人们在生产、生活中用量最大的无机非金属材料 | |
| C. | NO2、SO2、CO2、PM2.5都是空气质量日报必须报道的大气污染物 | |
| D. | 家用天然气含有特殊气味的主要原因是开采的天然气未经处理就直接转为民用燃气 |
分析 A.反应中有新物质生成的反应通常为化学变化;
B.无机非金属材是以某些元素的氧化物、碳化物、氮化物、卤素化合物、硼化物以及硅酸盐、铝酸盐、磷酸盐、硼酸盐等物质组成的材料.是除有机高分子材料和金属材料以外的所有材料的统称;
C.我国“城市空气质量日报”报道的污染物主要是SO2、氮氧化物和可吸入颗粒等指标;
D.天然气本身无色、无味,泄露不易察觉,需加入有特殊气味的物质便于人们及时发现天然气泄露.
解答 解:A.石油分馏得到汽油、柴油等是利用了物质的沸点不同而分离的方法,海水制盐没有新物质生成,属于物理变化,故A错误;
B.传统无机非金属材料,主要是硅酸盐工业,水泥、玻璃、陶瓷等都是无机非金属材料,故B正确;
C.动植物的呼吸作用能产生CO2是,而绿色植物进行光合作转变成O2,不属于“城市空气质量日报”报道的,故C错误;
D.天然气本身是一种无色、无味的气体,泄漏时难于察觉,使用时常在天然气中加入少量有特殊气味的乙硫醇,能便于人们及时发现天然气泄露,故D错误.
故选B.
点评 本题考查化学与环境、材料、信息、能源关系密切相关的知识,为高频考点,侧重于基础知识的综合理解和运用的考查,注意性质决定物质的用途,并把握化学与生活的联系,题目难度不大.

练习册系列答案
相关题目
10.在恒温恒容体系中建立平衡aA(g)?bB(g)+cC(g),若再加入A.
| 平衡移动方向 | A的转化率 | 解释 | |
| a=b+c | |||
| a>b+c | |||
| a<b+c |
9.在80℃时,将0.40mol 的N2O4气体充入2L 已经抽成真空的固定容积的密闭容器中,发生如下反应:N2O4(g)?2NO2 (g)△H=+56.9kJ/mol,隔一段时间对该容器内的物质进行分析,得到如下数据:
(1)反应进行至100s 后将反应混合物的温度降低,混合气体的颜色变浅(填“变浅”、“变深”或“不变”).
(2)20s时,N2O4的浓度为0.14mol/L,0~20s内N2O4的平均反应速率为0.003mol/(L.s).
(3)该反应的平衡常数表达式K=$\frac{{c}^{2}(N{O}_{2})}{c({N}_{2}{O}_{4})}$.
(4)在其他条件相同时,该反应的K值越大,表明建立平衡时ABD.(多选)
A.N2O4的转化率越高B.NO2的产量越大
C.N2O4与NO2的浓度之比越大D.正反应进行的程度越大
(5)要增大该反应的K值,可采取的措施有D(填序号).
A.增大N2O4起始浓度B.向混合气体中通入NO2C.使用高效催化剂D.升高温度
(6)当反应达到平衡后,下列操作,不能使平衡混合气体颜色加深的是D
A.恒温恒容下再通入N2O4气体
B.恒温恒容下再通入NO2气体
C.恒容时,升高温度
D.恒温恒容时通入Ar
E.恒温时压缩体积.
| n/mol 时间/s | 0 | 20 | 40 | 60] | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(2)20s时,N2O4的浓度为0.14mol/L,0~20s内N2O4的平均反应速率为0.003mol/(L.s).
(3)该反应的平衡常数表达式K=$\frac{{c}^{2}(N{O}_{2})}{c({N}_{2}{O}_{4})}$.
(4)在其他条件相同时,该反应的K值越大,表明建立平衡时ABD.(多选)
A.N2O4的转化率越高B.NO2的产量越大
C.N2O4与NO2的浓度之比越大D.正反应进行的程度越大
(5)要增大该反应的K值,可采取的措施有D(填序号).
A.增大N2O4起始浓度B.向混合气体中通入NO2C.使用高效催化剂D.升高温度
(6)当反应达到平衡后,下列操作,不能使平衡混合气体颜色加深的是D
A.恒温恒容下再通入N2O4气体
B.恒温恒容下再通入NO2气体
C.恒容时,升高温度
D.恒温恒容时通入Ar
E.恒温时压缩体积.
6.某化合物由两种单质直接反应生成,将其加入Ba(HCO3)2溶液中同时有气体和沉淀产生.下列化合物中符合上述条件的是( )
| A. | Na2O2 | B. | CaO | C. | FeCl2 | D. | SiO2 |
13.表中除杂所选用的试剂及操作方法均正确的一组是(括号内为杂质)( )
| 选项 | 待提纯的物质 | 选用试剂 | 操作方法 |
| A | Cu(Fe) | 稀盐酸 | 过滤 |
| B | CaO(CaCO3) | 盐酸 | 蒸发 |
| C | CO2(CO) | 石灰水 | 通入 |
| D | MgCl2溶液(盐酸) | 氢氧化钠溶液 | 滴加 |
| A. | A | B. | B | C. | C | D. | D |
10.实验中需要2.0mol/L的Na2CO3溶液950mL,配制时应选选用的容量瓶的规格和称取Na2CO3的质量分别是( )
| A. | 1000ml,212g | B. | 950ml 543.4g | C. | 950ml 201g | D. | 500ml 286g |
7.将4mol金属Al全部转化为Al(OH)3,共消耗HClamol,NaOHbmol,则(a+b)的最小值为( )
| A. | 4mol | B. | 6mol | C. | 8mol | D. | 16mol |
8.下列反应中,不属于四种基本反应类型的是( )
| A. | 2Na+2H2O═2NaOH+H2 | B. | CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 | ||
| C. | Fe+2FeCl3═3FeCl2 | D. | 2HCl$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑ |
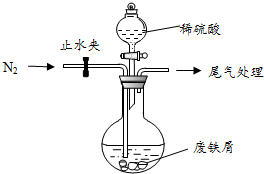 医疗上绿矾(FeSO4•7H2O)是治疗缺铁性贫血的特效药.某化学兴趣小组对绿矾进行了如下的探究:
医疗上绿矾(FeSO4•7H2O)是治疗缺铁性贫血的特效药.某化学兴趣小组对绿矾进行了如下的探究: