题目内容
下列有关实验操作正确的是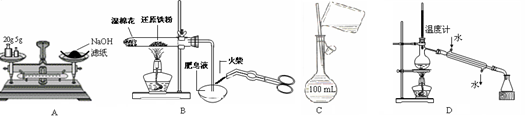
| A.称量氢氧化钠固体 | B.检验铁粉与水蒸气反应产生的氢气 |
| C.配制150 mL 0.10 mol/L盐酸 | D.分离两种互溶但沸点相差较大的液体混合物 |
B
解析试题分析:A、托盘天平的使用应该是左盘放物体右盘放砝码,氢氧化钠应在烧杯中称量,错误;C、配制150 mL 0.10 mol/L盐酸所选容量瓶容积不应为100mL,错误;D、冷凝管的水流方向应是下口进水上口出水,错误。
考点:考查化学实验基本操作

练习册系列答案
 名题金卷系列答案
名题金卷系列答案
相关题目
下列实验基本操作正确的是
| A.酸式滴定管洗净后直接装待装液 |
| B.用玻璃棒蘸取溶液滴到湿润的pH试纸上测其pH |
| C.用碱式滴定管量取0.10 mol·L-1的Na2CO3溶液22.10 mL |
| D.配制一定浓度的氢氧化钠溶液时,将氢氧化钠固体放在纸片上称量 |
下列操作中,不用玻璃棒的是
| A.过滤 | B.蒸发 | C.蒸馏 | D.溶解 |
下列关于仪器使用的说法正确的是
| A.量筒要准确量取一定体积的液体必须借助胶头滴管定容 |
| B.滴定管量取待测液后要用蒸馏水洗涤滴定管,洗液转入锥形瓶 |
| C.蒸馏时一定要用到蒸馏烧瓶和温度计 |
| D.振荡分液漏斗时应打开其上端玻璃塞并关闭下端活塞 |
用固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移溶液、定容等操作。下列图示对应的操作规范的是
| A.称量 | B.溶解 | C.转移 | D.定容 |
下列实验操作或描述中,错误的是
| A.将等物质的量的NaNO3和KCl的混合液加热并浓缩至有晶体析出,趁热过滤时,可分离出NaCl晶体 |
| B.亚硝酸银和氯化银都是白色沉淀,故不能用硝酸银和稀硝酸溶液来区别亚硝酸钠与氯化钠 |
| C.冷却结晶时,如未出现结晶,可以用玻璃棒摩擦瓶壁并将锥形瓶置于冰水中冷却,促使晶体析出 |
| D.在适量氯化钴的乙醇溶液中,逐滴加入水至溶液恰好呈粉红色,加热该溶液,结果依次呈现紫色、蓝紫色、蓝色的变化 |
研究物质的性质的基本程序是一个系统过程,其基本程序一般分为四个过程。下列是研究物质性质的基本程序的第一步的是
| A.预测物质的性质 | B.观察物质的外观状态 |
| C.进行实验和观察 | D.作出相关的解释和结论 |
下列说法不合理的是
| A.容量瓶、量筒和滴定管上都标有使用温度,量筒、容量瓶无“0”刻度,滴定管有“0”刻度;使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗 |
| B.在两支试管中分别加1mL无水乙醇和1.5g苯酚固体,再加等量等体积的钠,比较乙醇、苯酚羟基上氢原子的活泼性 |
| C.用纸上层析法检验氯化铁溶液中是否混有少量氯化铜 |
| D.硝酸钾饱和溶液冷却未出现结晶时,可以用玻棒充分摩擦器皿壁促使晶体析出 |