题目内容
下列微粒的核外电子的表示方法中正确的是( )
A、碳原子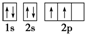 | B、P原子价电子轨道表示式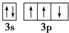 | C、Cr原子的价电子排布式3d44s1 | D、Fe2+价电子排布式3d44s2 |
分析:A.碳原子核外6个电子;
B.洪特规则是在等价轨道(相同电子层、电子亚层上的各个轨道)上排布的电子将尽可能分占不同的轨道,且自旋方向相同;
C.全空,全满,半满时能量最低;
D.铁原子在失电子时,先失去最外层的两个4s电子.
B.洪特规则是在等价轨道(相同电子层、电子亚层上的各个轨道)上排布的电子将尽可能分占不同的轨道,且自旋方向相同;
C.全空,全满,半满时能量最低;
D.铁原子在失电子时,先失去最外层的两个4s电子.
解答:解:A.碳原子核外6个电子,最外层4个电子,故A正确;
B.3p上的3个电子应自旋相同,故B错误;
C.全空,全满,半满时能量最低,正确的Cr原子的价电子排布式为3d54s1,故C错误;
D.铁原子在失电子时,先失去最外层的两个4s电子,电子排布为3d6,Fe2+价电子排布式3d6,故D错误.
故选A.
B.3p上的3个电子应自旋相同,故B错误;
C.全空,全满,半满时能量最低,正确的Cr原子的价电子排布式为3d54s1,故C错误;
D.铁原子在失电子时,先失去最外层的两个4s电子,电子排布为3d6,Fe2+价电子排布式3d6,故D错误.
故选A.
点评:本题考查原子核外电子的能级分布,难度不大,注意全空,全满,半满时能量最低.

练习册系列答案
相关题目
|
下列说法中正确的是 | |
| [ ] | |
A. |
某微粒的核外电子排布为 |
B. |
最外层电子达稳定结构的微粒只能是稀有气体的原子 |
C. |
F-、Na+、Mg2+、Al3+是与氖原子具有相同电子层结构的离子 |
D. |
NH4+、H3O+、OH-、Na+具有相同的质子数和电子数 |
下列微粒的核外电子的表示方法中正确的是( )
A.碳原子  |
B.P原子价电子轨道表示式 |
| C.Cr原子的价电子排布式 3d44s1 |
| D.Fe2+ 价电子排布式3d44s2 |
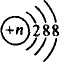 ,则该微粒一定是氩原子
,则该微粒一定是氩原子
