题目内容
关于下列各装置图的叙述中,不正确的是
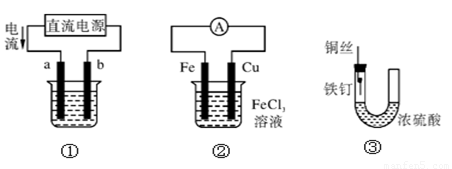
A.用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液
B.用装置①进行电镀,镀件接在b极上
C.装置②的总反应是:Cu+2Fe3+=Cu2++2Fe2+
D.装置③中的铁钉几乎没被腐蚀
【答案】
C
【解析】
试题分析:A.Cu精炼时粗铜作阳极,精铜作阴极,含有Cu2+的溶液作电解液。正确。B.若用用装置①进行电镀,则应该是镀层金属作阳极a,镀件作阴极,连接在直流电源的负极上,即连在b极上。正确。C.由于活动性Fe>Cu,所以在装置②的原电池反应中,Fe作负极,Cu作正极,总反应是:Fe+2Fe3+=3Fe2+。错误。D.因为Fe在常温下遇到浓硫酸、浓硝酸时会被氧化产生一薄层致密的氧化物薄膜,对内层的金属起到了保护作用,这种现象叫钝化。所以在装置③中的铁钉由于钝化几乎没被腐蚀。正确。
考点:考查原电池、电解池、电镀及金属的钝化等知识。

练习册系列答案
相关题目
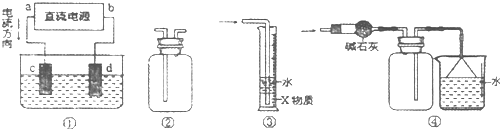
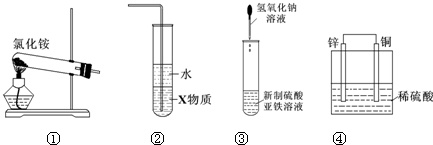
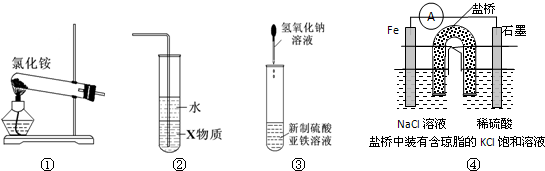
关于下列各装置图的叙述中,正确的是( )
A、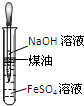 制取及观察Fe(OH)2 | B、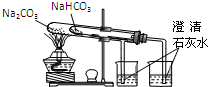 比较两种物质的热稳定性 | C、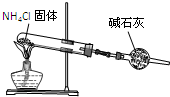 实验室制取NH3 | D、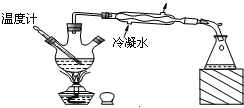 分离沸点不同且互溶的液体混合物. |