题目内容
 Ⅰ.下列各组物质是按一定规律排列的,请将对应的排列依据填在括号内.
Ⅰ.下列各组物质是按一定规律排列的,请将对应的排列依据填在括号内.
(1)N2H4、N2O、NO、HNO2、N2O4、HNO3(______)
(2)CH4、C2H6、C3H8、C4H10、C5H12 (______)
(3)Ca、Mg、Fe、Cu、Pt (______)
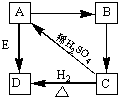
Ⅱ. A、B、C、D、E为常见物质,已知A溶液为蓝色,B是一种碱,C是碱性氧化物,D和E为金属单质,回答:
(1)写出A、B、C的化学式:A______;B______;C______;D______;E______
(2)写出下列各步的化学反应方程式:
A→B:______;
A→D:______.
Ⅲ.有人在研究硫酸亚铁(FeSO4)受热分解时,作出了两种假设:
(1)假设它按KClO3受热分解的方式分解,反应的化学方程式为______;
(2)假设它按CaCO3受热分解的方式分解,反应的化学方程式为______.
解:I、(1)N2H4、N2O、NO、HNO2、N2O4、HNO3中,N元素的化合价分别为-2、+1价、+2价、+3价、+4价、+5价,化合价依次升高,故答案为:氮元素的化合价依次升高;
(2)CH4、C2H6、C3H8、C4H10、C5H12 是按照分子组成依次增加1个“CH2”原子团的顺序排列,故答案为:分子组成依次增加1个“CH2”原子团;
(3)Ca、Mg、Fe、Cu、Pt按金属活动性逐渐减弱的顺序排列,故答案为:金属活动性依次减弱;
Ⅱ、(1)A溶液为蓝色,应含有Cu2+,B是一种碱,应为Cu(OH)2,C是碱性氧化物,应为CuO,根据转化关系可知D为Cu,A为CuSO4,E为金属单质,应为较Cu活泼的金属,可为
Fe,故答案为:CuSO4;Cu(OH)2;CuO;Cu;Fe;
(2)CuSO4和NaOH反应生成Cu(OH)2和Na2SO4,反应的化学方程式为CuSO4+2NaOH=Cu(OH)2↓+Na2SO4,CuSO4可与Fe反应生成Cu,反应的化学方程式为CuSO4+Fe=FeSO4+Cu,
故答案为:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;CuSO4+Fe=FeSO4+Cu;
Ⅲ、(1)硫酸亚铁按氯酸钾受热分解的方式来分解,那么产物是FeS和O2,即FeSO4 FeS+2O2↑,故答案为:FeSO4
FeS+2O2↑,故答案为:FeSO4 FeS+2O2↑;
FeS+2O2↑;
(2)硫酸亚铁按照碳酸钙受热分解的方式来分解生成FeO和SO3,方程式为:FeSO4 FeO+SO3↑,故答案为:FeSO4
FeO+SO3↑,故答案为:FeSO4 FeO+SO3↑.
FeO+SO3↑.
分析:I、(1)根据N元素的化合价判断;
(2)根据金属活动性顺序分析;
Ⅱ、A溶液为蓝色,应含有Cu2+,B是一种碱,应为Cu(OH)2,C是碱性氧化物,应为CuO,根据转化关系可知D为Cu,A为CuSO4,E为金属单质,应为较Cu活泼的金属,可为Fe,以此解答该题;
Ⅲ、(1)根据氯酸钾受热分解生成氯化钾和氧气的反应进行分析硫酸亚铁(FeSO4)受热分解反应;
(2)根据碳酸钙高温分解成氧化钙和二氧化碳的反应进行分析硫酸亚铁(FeSO4)分解反应,写出方程式.
点评:本题考查无机物的推断,题目难度不大,本题注意推断该题的突破口为“溶液为蓝色,B是一种碱,C是碱性氧化物”,此外还考查了化学方程式的书写,首先确定反应原理,然后再依据原理找出反应物、生成物和反应条件,根据方程式的书写规则书写方程式.
(2)CH4、C2H6、C3H8、C4H10、C5H12 是按照分子组成依次增加1个“CH2”原子团的顺序排列,故答案为:分子组成依次增加1个“CH2”原子团;
(3)Ca、Mg、Fe、Cu、Pt按金属活动性逐渐减弱的顺序排列,故答案为:金属活动性依次减弱;
Ⅱ、(1)A溶液为蓝色,应含有Cu2+,B是一种碱,应为Cu(OH)2,C是碱性氧化物,应为CuO,根据转化关系可知D为Cu,A为CuSO4,E为金属单质,应为较Cu活泼的金属,可为
Fe,故答案为:CuSO4;Cu(OH)2;CuO;Cu;Fe;
(2)CuSO4和NaOH反应生成Cu(OH)2和Na2SO4,反应的化学方程式为CuSO4+2NaOH=Cu(OH)2↓+Na2SO4,CuSO4可与Fe反应生成Cu,反应的化学方程式为CuSO4+Fe=FeSO4+Cu,
故答案为:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;CuSO4+Fe=FeSO4+Cu;
Ⅲ、(1)硫酸亚铁按氯酸钾受热分解的方式来分解,那么产物是FeS和O2,即FeSO4
 FeS+2O2↑,故答案为:FeSO4
FeS+2O2↑,故答案为:FeSO4 FeS+2O2↑;
FeS+2O2↑;(2)硫酸亚铁按照碳酸钙受热分解的方式来分解生成FeO和SO3,方程式为:FeSO4
 FeO+SO3↑,故答案为:FeSO4
FeO+SO3↑,故答案为:FeSO4 FeO+SO3↑.
FeO+SO3↑.分析:I、(1)根据N元素的化合价判断;
(2)根据金属活动性顺序分析;
Ⅱ、A溶液为蓝色,应含有Cu2+,B是一种碱,应为Cu(OH)2,C是碱性氧化物,应为CuO,根据转化关系可知D为Cu,A为CuSO4,E为金属单质,应为较Cu活泼的金属,可为Fe,以此解答该题;
Ⅲ、(1)根据氯酸钾受热分解生成氯化钾和氧气的反应进行分析硫酸亚铁(FeSO4)受热分解反应;
(2)根据碳酸钙高温分解成氧化钙和二氧化碳的反应进行分析硫酸亚铁(FeSO4)分解反应,写出方程式.
点评:本题考查无机物的推断,题目难度不大,本题注意推断该题的突破口为“溶液为蓝色,B是一种碱,C是碱性氧化物”,此外还考查了化学方程式的书写,首先确定反应原理,然后再依据原理找出反应物、生成物和反应条件,根据方程式的书写规则书写方程式.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案
相关题目
 Ⅰ.下列各组物质是按一定规律排列的,请将对应的排列依据填在括号内.
Ⅰ.下列各组物质是按一定规律排列的,请将对应的排列依据填在括号内. ( I)下列各组物质是按一定规律排列的,请将对应的排列依据填在括号内.
( I)下列各组物质是按一定规律排列的,请将对应的排列依据填在括号内.