题目内容
以下是依据一定的分类标准对某些物质与水反应的情况进行分类的分类图.请根据你所学的知识,按要求填空.
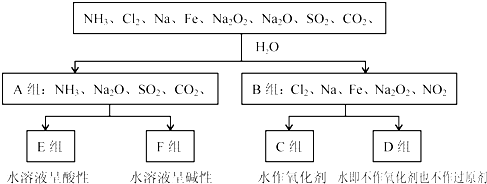
上述第一次分类标准时(分A、B组的依据)是______.
(2)C组中的某一物质在常温下能与冷水反应,反应的化学方程式为:______.
(3)D组中与水反应氧化剂与还原剂的之比是1:1除了氯气外还有______(填化学式).
(4)由Al3+制备Al(OH)3最好选择F组中的氨水,用离子方程式说明原理:______.
(5)SO2、Cl2、Na2O2都能使品红褪色,其漂白原理不同的是______.等物质的量的SO2、Cl2同时通入到使品红溶液,实验现象是______.用化学方程式说明原理:______.

上述第一次分类标准时(分A、B组的依据)是______.
(2)C组中的某一物质在常温下能与冷水反应,反应的化学方程式为:______.
(3)D组中与水反应氧化剂与还原剂的之比是1:1除了氯气外还有______(填化学式).
(4)由Al3+制备Al(OH)3最好选择F组中的氨水,用离子方程式说明原理:______.
(5)SO2、Cl2、Na2O2都能使品红褪色,其漂白原理不同的是______.等物质的量的SO2、Cl2同时通入到使品红溶液,实验现象是______.用化学方程式说明原理:______.
(1)溶于水分成AB两组的依据,分析反应过程可知,NH3、Na2O、SO2、CO2溶于水发生化合反应生成对应酸或碱,是非氧化还原反应;Cl2、Na、Fe、Na2O、NO2,溶于水反应发生的是氧化还原反应,所以依据是否发生氧化还原反应,故答案为:是否发生氧化还原反应;
(2)水在氧化还原反应中作氧化剂,则该物质作还原剂,且在常温下能与水反应只有钠,反应的方程式为:2Na+2H2O=2NaOH+H2↑,故答案为:2Na+2H2O=2NaOH+H2↑;
(3)过氧化钠与水反应时氧化剂与还原剂的之比是1:1,
故答案为:Na2O2;
(4)氢氧化铝是两性氢氧化物溶于过量的强碱,但不溶于弱碱,方程式为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故答案为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+;
(5)SO2、Cl2、Na2O2的漂白原理分别是化合漂白、氧化漂白、氧化漂白,所以其漂白原理不同的是SO2,故答案为:SO2;
等物质的量的SO2、Cl2同时通入到使品红溶液,发生反应:SO2+Cl2+2H2O=H2SO4+2HCl,硫酸和盐酸均无漂白性,所以品红溶液不褪色,
故答案为:品红溶液不褪色;SO2+Cl2+2H2O=H2SO4+2HCl.
(2)水在氧化还原反应中作氧化剂,则该物质作还原剂,且在常温下能与水反应只有钠,反应的方程式为:2Na+2H2O=2NaOH+H2↑,故答案为:2Na+2H2O=2NaOH+H2↑;
(3)过氧化钠与水反应时氧化剂与还原剂的之比是1:1,
故答案为:Na2O2;
(4)氢氧化铝是两性氢氧化物溶于过量的强碱,但不溶于弱碱,方程式为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故答案为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+;
(5)SO2、Cl2、Na2O2的漂白原理分别是化合漂白、氧化漂白、氧化漂白,所以其漂白原理不同的是SO2,故答案为:SO2;
等物质的量的SO2、Cl2同时通入到使品红溶液,发生反应:SO2+Cl2+2H2O=H2SO4+2HCl,硫酸和盐酸均无漂白性,所以品红溶液不褪色,
故答案为:品红溶液不褪色;SO2+Cl2+2H2O=H2SO4+2HCl.

练习册系列答案
相关题目
