题目内容
下列顺序正确的是( )
| A.熔点:SiO2< NaF<KCl | B.水溶性:NH3<SO2<HCl |
| C.酸性:HF>HCl>HI | D.碱性:Mg(OH)2<KOH<RbOH |
D
试题分析:A. 一般情况下物质的熔沸点:原子晶体>离子晶体>分子晶体。SiO2 是原子晶体,原子间通过共价键结合,共价键是一种强烈的相互作用,断裂较难,因此熔沸点高,而NaF、KCl都是离子晶体,离子键NaF>KCl.离子键越强,断裂越难,该物质的熔沸点就越高。所以这几种物质的熔点: SiO2 >NaF>KCl。错误。B.水溶性:NH3:1:700;SO2:1:40;HCl :1:500.所以水溶性NH3 >HCl >SO2。错误。D.元素的金属性越强,其相应的氢氧化物的碱性就越强,由于元素的金属性:Rb>K>Mg.所以碱性:Mg(OH)2<KOH<RbOH。正确。

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目

 ,从而对人体产生危害。该同位素原子的中子数和质子数之差为
,从而对人体产生危害。该同位素原子的中子数和质子数之差为 
 )。它们满足如图转化关系,则下列说法正确的是( )
)。它们满足如图转化关系,则下列说法正确的是( )
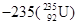 是制造原子弹的燃料。
是制造原子弹的燃料。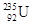 原子核内含有中子数为
原子核内含有中子数为