题目内容
【题目】铁电池是一种新兴的化学电源,总反应方程式:3Zn+2FeO42-+8H2O= 3Zn(OH)2↓+ 2Fe(OH)3↓+4OH-,其工作示意图如下。

下列说法不正确的是( )
A. Zn极上发生氧化反应
B. 电解质溶液中电子由左侧向右侧转移
C. 正极的电极反应式:FeO42-+3e-+4H2O=Fe(OH)3+5OH-
D. 反应一段时间后,Zn极质量减少6.5g,假设反应前后溶液体积不变仍为100 mL,则OH-浓度约增大了 1.33 mol·L-1
【答案】B
【解析】A. 根据方程式,锌反应后化合价升高,被氧化,为负极,发生氧化反应,故A正确;B. 在原电池中,电子不能通过电解质溶液,电解质溶液是通过离子导电的,故B错误;C.根据方程式,正极上FeO42-发生还原反应,电极反应式:FeO42-+3e-+4H2O=Fe(OH)3+5OH-,故C正确;D. Zn极质量减少6.5g,反应的锌的物质的量为0.1mol,转移0.2mol电子,根据方程式,反应生成的氢氧根离子为![]() ×0.1mol=
×0.1mol=![]() mol,若反应后溶液体积仍为100 mL,则OH-浓度约增大了
mol,若反应后溶液体积仍为100 mL,则OH-浓度约增大了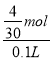 =1.33 mol·L-1,故D正确;故选B。
=1.33 mol·L-1,故D正确;故选B。

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目

