题目内容
实验室所使用的NaOH标准溶液,通常是用准确称量的邻苯二甲酸氢钾(相对分子质量为204)来“标定”的。其操作步骤如下:①将用分析天平称好的邻苯二甲酸氢钾置于锥形瓶中 ②加适量的蒸馏水溶解,溶液呈无色 ③加入指示剂 ④用NaOH溶液滴定到终点
某学生进行了三次平行实验,实验数据如下:
实验编号 | 邻苯二甲酸氢钾的质量(g) | 待测NaOH溶液的体积(mL) |
1 | 0.612 | 21.20 |
2 | 0.612 | 20.10 |
3 | 0.612 | 19.90 |
试完成下列问题
(1)邻苯二甲酸氢钾与NaOH溶液反应的离子方程式是_______________________________。
(2)所加指示剂最好选用_____________(填“甲基橙”“酚酞”或“石蕊”)判断达到终点的标志是________________________________________________________________。
(3)该同学在进行滴定时,左手应该___________________,右手应该____________________,眼睛应该___________________。
(4)第_________次实验误差较大,造成这种误差的可能原因是( )
A.碱式滴定管在装NaOH溶液前未用待测NaOH溶液润洗2—3次
B.滴定过程中,振荡太剧烈以致有些溶液飞溅出来
C.滴定开始前尖嘴部分有气泡,在滴定终点读数时没有了气泡
D.达到滴定终点时,俯视读数
(5)该同学所“标定”的NaOH溶液的物质的量浓度为_________mol·L-1(结果保留三位数)。
![]() (也可用“
(也可用“![]() ”)
”)
(2)酚酞 当滴加最后一滴NaOH溶液时,溶液由无色突变为粉红色,并半分钟内不褪色
(3)挤压橡皮管玻璃球 振荡锥形瓶 注视溶液颜色的变化和滴定管流速
(4)1 AC
(5)0.150
解析:(1)邻苯二甲酸氢钾应写成离子形式。
(2)酚酞在滴定终点时色差明显,灵敏度高。
(3)左手控制的是碱式滴定管,右手摇晃锥形瓶,眼睛紧盯锥形瓶中溶液的颜色变化。
(4)第1次与2、3次差别较大,由误差引起,消耗NaOH溶液偏多,A、C都有可能,B导致消耗NaOH溶液偏少,D导致读数偏小。
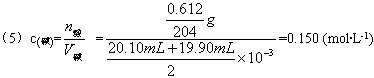

| A、测定硫酸铜晶体中结晶水含量,失水后的硫酸铜置于空气中冷却后再测质量 | B、测定中和热实验中,所使用的NaOH稀溶液的物质的量浓度稍大于稀盐酸 | C、配制一定物质的量浓度溶液的实验中,容量瓶内壁附有蒸馏水 | D、用标准盐酸滴定未知浓度的氢氧化钠溶液,开始时俯视读数,终点时仰视读数 |
①将用分析天平称好的邻苯二甲酸氢钾置于锥形瓶中 ②加适量的蒸馏水溶解,溶液呈无色 ③加入指示剂 ④用NaOH溶液滴定到终点?
某学生进行了三次平行实验,实验数据如下:?
实验编号 | 邻苯二甲酸氢钾的质量/g | 待测NaOH溶液的体积/mL |
1 | 0.612 | 21.20 |
2 | 0.612 | 20.10 |
3 | 0.612 | 19.90 |
试回答下列问题:?
(1)邻苯二甲酸氢钾与NaOH溶液反应的离子方程式是 。?
(2)所加指示剂最好选用 (填“甲基橙”“酚酞”或“石蕊”),判断达到终点的标志是________。
(3)该同学在进行滴定时,左手应该 ,右手应该 ,眼睛应该 。?
(4)第 次实验误差较大,造成这种误差的可能原因是 。?
A碱式滴定管在装NaOH溶液前未用待测NaOH溶液润洗2~3次?
B滴定过程中,振荡太剧烈以致有些溶液飞溅出来?
C滴定开始前尖嘴部分有气泡,在滴定终点读数时没有了气泡?
D达到滴定终点时,俯视读数?
(5)该同学所“标定”的NaOH溶液的物质的量浓度为? ?mol·L-1(结果保留三数)。