题目内容
被称为万能还原剂的NaBH4溶于水并和水反应:NaBH4+2H2O=NaBO2+4H2↑,下列说法中不正确的是(NaBH4中H为-1价)
- A.硼元素在反应前后化合价不变
- B.NaBH4是还原剂,H2O是氧化剂
- C.被氧化的元素与被还原的元素质量之比为1:1
- D.生成标准状况下22.4L的氢气,转移2mol电子
D
分析:在NaBH4+2H2O=NaBO2+4H2↑反应中,NaBH4中H元素的化合价为-1价,H2O中H元素的化合价为+1价,二者发生氧化还原反应,其中NaBH4是还原剂,H2O是氧化剂.
解答:A.硼元素在反应前后化合价不变,都是+3价,故A正确;
B.该反应中NaBH4失电子作还原剂,H2O得电子作氧化剂,故B正确;
C.反应中B元素的化合价没有发生变化,反应中氧化剂和还原剂中化合价变化的数值相等,则被氧化的元素与被还原的元素质量比为1:1,故C正确;
D.生成标准状况下22.4L的氢气,转移1mol电子,故D错误;
故选D.
点评:本题考查氧化还原反应,注意NaBH4中H元素的化合价是-1价,会根据化合价的变化计算电子转移的数目,难度不大.
分析:在NaBH4+2H2O=NaBO2+4H2↑反应中,NaBH4中H元素的化合价为-1价,H2O中H元素的化合价为+1价,二者发生氧化还原反应,其中NaBH4是还原剂,H2O是氧化剂.
解答:A.硼元素在反应前后化合价不变,都是+3价,故A正确;
B.该反应中NaBH4失电子作还原剂,H2O得电子作氧化剂,故B正确;
C.反应中B元素的化合价没有发生变化,反应中氧化剂和还原剂中化合价变化的数值相等,则被氧化的元素与被还原的元素质量比为1:1,故C正确;
D.生成标准状况下22.4L的氢气,转移1mol电子,故D错误;
故选D.
点评:本题考查氧化还原反应,注意NaBH4中H元素的化合价是-1价,会根据化合价的变化计算电子转移的数目,难度不大.

练习册系列答案
相关题目
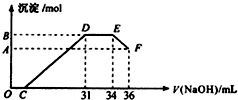 实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.现有一定量铝粉和铁粉的混合物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol?L-1 NaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示.
实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.现有一定量铝粉和铁粉的混合物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol?L-1 NaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示.