题目内容
在537℃、1.01×105Pa时,往容积可变的密闭容器中充入1mol X和3mol Y,此时容积为V L.保持恒温恒压,发生反应X(g)+3Y(g)
2Z(g),达到平衡时,平衡混合气体中Z的体积分数为0.5.
(1)达到平衡时,X的转化率约为
(2)保持上述温度和压强恒定不变,若向容器中只充入4mol Z,则反应达到平衡时,平衡气体中Y 的体积分数为
L.
(3)若另选一容积固定不变的密闭容器,仍控制温度不变,使2mol X和6mol Y反应,达到平衡时平衡气体中Z的体积分数仍为0.5,则该密闭容器的容积为
L.
(4)若温度仍为537℃,容器体积保持VL不变(恒容),往其中充入a mol X的b mol Y,使反应达到平衡,这时平衡气体中Z的体积分数仍为0.5,体系压强为1.01×105Pa,若a:b=1:3,则a=
(1)达到平衡时,X的转化率约为
66.7%
66.7%
.(2)保持上述温度和压强恒定不变,若向容器中只充入4mol Z,则反应达到平衡时,平衡气体中Y 的体积分数为
37.5%
37.5%
,容器的容积为| 4V |
| 3 |
| 4V |
| 3 |
(3)若另选一容积固定不变的密闭容器,仍控制温度不变,使2mol X和6mol Y反应,达到平衡时平衡气体中Z的体积分数仍为0.5,则该密闭容器的容积为
| 4V |
| 3 |
| 4V |
| 3 |
(4)若温度仍为537℃,容器体积保持VL不变(恒容),往其中充入a mol X的b mol Y,使反应达到平衡,这时平衡气体中Z的体积分数仍为0.5,体系压强为1.01×105Pa,若a:b=1:3,则a=
1.5mol
1.5mol
.分析:恒压下 X(g)+3Y(g)
2Z(g),
开始 1 3 0
转化 x 3x 2x
平衡1-x 3-3x 2x
到平衡时,平衡混合气体中Z的体积分数为0.5,
则
=0.5,解得x=
mol,以此结合等效平衡来解答该题.
开始 1 3 0
转化 x 3x 2x
平衡1-x 3-3x 2x
到平衡时,平衡混合气体中Z的体积分数为0.5,
则
| 2x |
| 4-2x |
| 2 |
| 3 |
解答:解:恒压下 X(g)+3Y(g)
2Z(g),
开始 1 3 0
转化 x 3x 2x
平衡 1-x 3-3x 2x
到平衡时,平衡混合气体中Z的体积分数为0.5,
则
=0.5,解得x=
mol,
(1)X的转化率约为
×100%=66.7%,故答案为:66.7%;
(2)保持上述温度和压强恒定不变,若向容器中只充入4molZ,与上述平衡等效,
则Y的体积分数为
×100%=37.5%,
由物质的量与体积成正比可知,设平衡的体积为x,则
=
,解得x=
L,故答案为:37.5%;
;
(3)容积固定不变的密闭容器,仍控制温度不变,使2mol X和6mol Y反应,达到平衡时平衡气体中Z的体积分数仍为0.5,
与加入4molZ建立的平衡等效,体积为
L,故答案为:
;
(4)容器体积保持VL不变(恒容),往其中充入a mol X的b mol Y,使反应达到平衡,这时平衡气体中Z的体积分数仍为0.5,体系压强为1.01×105Pa,若a:b=1:3,则 X(g)+3Y(g)
2Z(g),
开始 a 3a 0
转化 x 3x 2x
平衡a-x 3a-3x 2x
到平衡时,平衡混合气体中Z的体积分数为0.5,
=0.5,4a-2x=4mol,
解得a=1.5mol,故答案为:1.5mol.
开始 1 3 0
转化 x 3x 2x
平衡 1-x 3-3x 2x
到平衡时,平衡混合气体中Z的体积分数为0.5,
则
| 2x |
| 4-2x |
| 2 |
| 3 |
(1)X的转化率约为
| ||
| 1mol |
(2)保持上述温度和压强恒定不变,若向容器中只充入4molZ,与上述平衡等效,
则Y的体积分数为
3-3×
| ||
4-2×
|
由物质的量与体积成正比可知,设平衡的体积为x,则
| 4 |
| V |
| ||
| x |
| 4V |
| 3 |
| 4V |
| 3 |
(3)容积固定不变的密闭容器,仍控制温度不变,使2mol X和6mol Y反应,达到平衡时平衡气体中Z的体积分数仍为0.5,
与加入4molZ建立的平衡等效,体积为
| 4V |
| 3 |
| 4V |
| 3 |
(4)容器体积保持VL不变(恒容),往其中充入a mol X的b mol Y,使反应达到平衡,这时平衡气体中Z的体积分数仍为0.5,体系压强为1.01×105Pa,若a:b=1:3,则 X(g)+3Y(g)
开始 a 3a 0
转化 x 3x 2x
平衡a-x 3a-3x 2x
到平衡时,平衡混合气体中Z的体积分数为0.5,
| 2x |
| 4a-2x |
解得a=1.5mol,故答案为:1.5mol.
点评:本题考查化学平衡的计算及等效平衡,注意化学平衡三段法的计算及等效平衡的条件、体积与物质的量的关系即可解答,题目难度较大.

练习册系列答案
相关题目
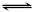 2Z(g),达到平衡时,平衡混合气体中Z的体积分数为0.5。
2Z(g),达到平衡时,平衡混合气体中Z的体积分数为0.5。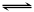 2Z(g),达到平衡时,平衡混合气体中Z的体积分数为0.5。
2Z(g),达到平衡时,平衡混合气体中Z的体积分数为0.5。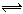 2Z(g),达到平衡时,平衡混合气体中Z的体积分数为0.5。
2Z(g),达到平衡时,平衡混合气体中Z的体积分数为0.5。