题目内容
【题目】铁被誉为“第一金属”,铁及其化合物在生活中有广泛应用。
![]() 的熔点为
的熔点为![]() ,沸点为
,沸点为![]() 的晶体类型是 ______ ;
的晶体类型是 ______ ;
![]() 羰基铁
羰基铁![]() 可用作催化剂、汽油抗爆剂等。1mol
可用作催化剂、汽油抗爆剂等。1mol![]() 分子中含______
分子中含______![]() 键;
键;
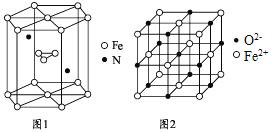
![]() 氮化铁晶体的晶胞结构如图1所示。该晶体中铁、氮的微粒个数之比为 ______ ;
氮化铁晶体的晶胞结构如图1所示。该晶体中铁、氮的微粒个数之比为 ______ ;
![]() 氧化亚铁晶体的晶胞如图2所示。已知:
氧化亚铁晶体的晶胞如图2所示。已知:
氧化亚铁晶体的密度为![]() ,
,![]() 代表阿伏加德罗常数的值。在该晶胞中,与
代表阿伏加德罗常数的值。在该晶胞中,与![]() 紧邻且等距离的
紧邻且等距离的![]() 数目为 ______ ;
数目为 ______ ;![]() 与
与![]() 最短核间距为 ______ pm。
最短核间距为 ______ pm。![]() 写出表达式
写出表达式![]()
【答案】 分子晶体 10 3:1 12 ![]() 1010
1010
【解析】(1)FeCl3的熔沸点较低,FeCl3的晶体类型是分子晶体。
(2)CO的结构式为C![]() O,三键中含1个σ键和2个π键,中心原子Fe与配体CO之间形成配位键,配位键也是σ键。
O,三键中含1个σ键和2个π键,中心原子Fe与配体CO之间形成配位键,配位键也是σ键。
(3)用“均摊法”确定晶胞中铁、氮的个数。
(4)根据晶胞,Fe2+为面心立方,与Fe2+紧邻的等距离的Fe2+有12个。由晶体的密度计算1mol晶体的体积,结合晶胞中所含微粒数计算晶胞的体积,用立体几何知识计算晶胞边长和Fe2+与O2-的最短核间距。
(1)FeCl3的熔沸点较低,FeCl3的晶体类型是分子晶体。
(2)CO的结构式为C![]() O,三键中含1个σ键和2个π键,中心原子Fe与配体CO之间形成配位键,配位键也是σ键;1个Fe(CO)5分子中含10个σ键,1molFe(CO)5分子中含10molσ键。
O,三键中含1个σ键和2个π键,中心原子Fe与配体CO之间形成配位键,配位键也是σ键;1个Fe(CO)5分子中含10个σ键,1molFe(CO)5分子中含10molσ键。
(3)用“均摊法”,晶胞中含Fe:12![]() +2
+2![]() +3=6个,N:2个,该晶体中铁、氮的微粒个数之比为6:2=3:1。
+3=6个,N:2个,该晶体中铁、氮的微粒个数之比为6:2=3:1。
(4)根据晶胞,Fe2+为面心立方,与Fe2+紧邻的等距离的Fe2+有12个。用“均摊法”,晶胞中含Fe2+:8![]() +6
+6![]() =4个,含O2-:12
=4个,含O2-:12![]() +1=4个,晶体的化学式为FeO;1molFeO的质量为72g,1mol晶体的体积为
+1=4个,晶体的化学式为FeO;1molFeO的质量为72g,1mol晶体的体积为![]() cm3;晶胞的体积为
cm3;晶胞的体积为![]() cm3
cm3![]() NA
NA![]() 4=
4=![]() cm3,晶胞的边长为
cm3,晶胞的边长为![]() cm,Fe2+与O2-最短核间距为
cm,Fe2+与O2-最短核间距为![]() cm=
cm=![]() cm=
cm=![]() 1010pm。
1010pm。

 阅读快车系列答案
阅读快车系列答案