题目内容
(2011?静安区模拟)大气固氮(闪电时N2转化为NO)和工业固氮(合成氨)是固氮的重要形式.下表列举了不同温度下大气固氮和工业固氮的部分K值(K表示平衡常数):
(1)固氮是指
(2)根据表中的数据,并结合所学知识分析,下列说法正确的是
a.人类大规模模拟大气固氮实际意义很小
b.常温下,大气固氮与工业固氮完成程度相差很大
c.两种固氮都是放热反应 d.在常温下,大气固氮几乎不可能,而工业固氮很容易进行
(3)为研究反应条件的改变对化学平衡移动的影响,将N2和H2在一固定体积的密闭容器中进行反应,得到如下的图象.下列有关条件改变(每次只改变一个条件)的说法,正确的是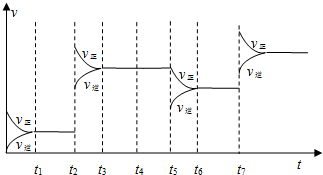
a.t2可能是增加了原料的物质的量
b.t4可能是充入了He气
c.t5是从反应体系中分离出氨气
d.t7时可能是升高温度,使平衡向正反应方向移动
(4)目前工业固氮采用的是哈伯法,即在20~50MPa的高压和500℃左右的高温下,并用铁触媒作为催化剂.俄勒冈大学的化学家使用了一种名为trans-Fe(DMeOPrPE)的新催化剂,在常温下合成氨,反应的化学方程式为:N2+3H2?2NH3.有关说法正确的是
a.新法不需要高温条件,可节约大量能源
b.新法能在常温下进行是因为不需要断裂化学键
c.在相同温度下不同的催化剂其催化活性不同.
| N2+O2?2NO | N2+3H2?2NH3 | |||
| 温度 | 25℃ | 2000℃ | 25℃ | 400℃ |
| K | 3.84×10-31 | 0.1 | 5×108 | 200 |
把大气中游离态的氮转化为氮的化合物
把大气中游离态的氮转化为氮的化合物
的过程,自然界固氮的另一途径为生物固氮
生物固氮
.(2)根据表中的数据,并结合所学知识分析,下列说法正确的是
a、b
a、b
.a.人类大规模模拟大气固氮实际意义很小
b.常温下,大气固氮与工业固氮完成程度相差很大
c.两种固氮都是放热反应 d.在常温下,大气固氮几乎不可能,而工业固氮很容易进行
(3)为研究反应条件的改变对化学平衡移动的影响,将N2和H2在一固定体积的密闭容器中进行反应,得到如下的图象.下列有关条件改变(每次只改变一个条件)的说法,正确的是
b、c
b、c
.
a.t2可能是增加了原料的物质的量
b.t4可能是充入了He气
c.t5是从反应体系中分离出氨气
d.t7时可能是升高温度,使平衡向正反应方向移动
(4)目前工业固氮采用的是哈伯法,即在20~50MPa的高压和500℃左右的高温下,并用铁触媒作为催化剂.俄勒冈大学的化学家使用了一种名为trans-Fe(DMeOPrPE)的新催化剂,在常温下合成氨,反应的化学方程式为:N2+3H2?2NH3.有关说法正确的是
a、c
a、c
.a.新法不需要高温条件,可节约大量能源
b.新法能在常温下进行是因为不需要断裂化学键
c.在相同温度下不同的催化剂其催化活性不同.
分析:(1)根据固氮的概念完成,根据常见的自然界固氮知识完成;
(2)根据表中的数据,并结合所学知识进行分析;
(3)根据图象及平衡移动原理进行判断;
(4)根据合成氨的反应原理及平衡移动原理分析.
(2)根据表中的数据,并结合所学知识进行分析;
(3)根据图象及平衡移动原理进行判断;
(4)根据合成氨的反应原理及平衡移动原理分析.
解答:解:(1)把大气中游离态的氮转化为氮的化合物称作固氮,自然界固氮的另一途径为生物固氮,
故答案是:把大气中游离态的氮转化为氮的化合物;生物固氮;
(2)a、比较大气固氮和工业固氮的平衡常数可知工业固氮比大规模模拟大气固氮要容易的多,所以大规模模拟大气固氮的实际意义很小,故a正确;
b、比较平衡常数可知大气固氮与工业固氮的平衡常数相差很大,故二者的完成程度相差也很大,故b正确;
c、比较不同温度下的平衡常数,可知大气固氮是吸热反应,而工业固氮是放热反应,故c错误;
d、常温下,从平衡常数看,常温下虽然工业固氮的平衡常数很大,但是仍需要高压和催化剂的作用,所以说很容易进行是不对滴,故d错误;
故选a、b;
(3)a、t2时若是增加原料,平衡向右移动,正反应速率迅速增加,逆反应速率开始不变,然后增大,应当是连续性的增大,而不会出现跳跃性的增加,故a错误;
b、t4加入He气,由于体题系是固定体积的密闭容器,所以充入He,平衡不移动,故b正确;
c、t5时从体系分离出氨气,逆反应速率跳跃性减小,正反应速率开始不变而后慢慢减小,符合图中图形,故c正确;
d、t7升高温度,正逆反应速率都增大,平衡向逆反应方向移动,v逆应当在v正的上面,和图形不符合,故d错误;
故选b、c;
(4)a、题目给出信息“在常温下合成氨”,所以不需要高温条件,可节约大量能源,故a正确;
b、任何化学反应都涉及旧键的断裂和新键的生成,故b错误;
c、相同温度下不同催化剂的催化活性不同,故c正确;
故选a、c.
故答案是:把大气中游离态的氮转化为氮的化合物;生物固氮;
(2)a、比较大气固氮和工业固氮的平衡常数可知工业固氮比大规模模拟大气固氮要容易的多,所以大规模模拟大气固氮的实际意义很小,故a正确;
b、比较平衡常数可知大气固氮与工业固氮的平衡常数相差很大,故二者的完成程度相差也很大,故b正确;
c、比较不同温度下的平衡常数,可知大气固氮是吸热反应,而工业固氮是放热反应,故c错误;
d、常温下,从平衡常数看,常温下虽然工业固氮的平衡常数很大,但是仍需要高压和催化剂的作用,所以说很容易进行是不对滴,故d错误;
故选a、b;
(3)a、t2时若是增加原料,平衡向右移动,正反应速率迅速增加,逆反应速率开始不变,然后增大,应当是连续性的增大,而不会出现跳跃性的增加,故a错误;
b、t4加入He气,由于体题系是固定体积的密闭容器,所以充入He,平衡不移动,故b正确;
c、t5时从体系分离出氨气,逆反应速率跳跃性减小,正反应速率开始不变而后慢慢减小,符合图中图形,故c正确;
d、t7升高温度,正逆反应速率都增大,平衡向逆反应方向移动,v逆应当在v正的上面,和图形不符合,故d错误;
故选b、c;
(4)a、题目给出信息“在常温下合成氨”,所以不需要高温条件,可节约大量能源,故a正确;
b、任何化学反应都涉及旧键的断裂和新键的生成,故b错误;
c、相同温度下不同催化剂的催化活性不同,故c正确;
故选a、c.
点评:本题考查了固氮知识、合成氨的条件选择等知识,涉及的题量较大,根据平衡移动原理进行分析即可,难度中等.

练习册系列答案
相关题目
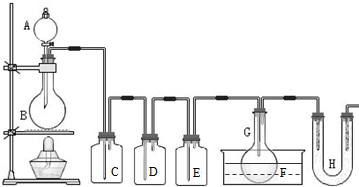 (2011?静安区模拟)用如图所示装置制取PCl3,在E中放入足量白磷,将氯气不间断地通入E,氯气与白磷就会发生反应,并放出热量(温度高于75℃).已知:PCl3和 PCl5遇水强烈反应,它们熔沸点数据如下:
(2011?静安区模拟)用如图所示装置制取PCl3,在E中放入足量白磷,将氯气不间断地通入E,氯气与白磷就会发生反应,并放出热量(温度高于75℃).已知:PCl3和 PCl5遇水强烈反应,它们熔沸点数据如下: