题目内容
下列叙述正确的是
①7Li+中含有的中子数与电子数之比为2︰1
② 在C2H6分子中极性共价键与非极性共价键数之比为3︰1
③ 常温下,11.2 L的甲烷气体中含有的氢、碳原子数之比为4︰1
④5.6 g铁与足量的氯气反应失去的电子与参与反应的铁的物质的量之比为2︰1
| A.①② | B.②③ | C.①③ | D.③④ |
C
解析试题分析:①7Li+中含有的中子数是4,电子数是2,之比为2:1,正确;②C2H6分子中极性共价键数是6,非极性共价键数是1,之比为6:1,错误;③甲烷的分子组成与条件、体积无关,氢、碳原子数之比始终是为4︰1,正确;④铁与足量的氯气反应生成氯化铁,所以5.6g铁失去电子的物质的量为0.3mol,参与反应的铁的物质的量为0.1mol,之比为3:1,错误,答案选C。
考点:考查微粒的中子数与电子数的计算,极性共价键与非极性共价键数比、分子中原子个数比、转移电子数的计算

 精英口算卡系列答案
精英口算卡系列答案在含有n mol FeI2的溶液中通入Cl2,有x mol Cl2发生反应。下列说法正确的是
A.当x ≤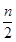 时,反应的离子方程式为:2Fe2++ Cl2 → 2Fe3++ 2Cl- 时,反应的离子方程式为:2Fe2++ Cl2 → 2Fe3++ 2Cl- |
| B.当x ≥ n时,反应的离子方程式为:2Fe2++ 2I-+ 2Cl2 → 2Fe3++ I2+ 4Cl- |
| C.当Fe2+和I-同时被氧化时,x与n的关系为x>n |
| D.当x=n时,反应后氧化产物的物质的量为n mol |
在100mL混合酸的溶液中,硝酸的物质的量浓度为0.4mol/L,硫酸的物质的量浓度为0.2mol/L,向其中加入6.4g铜粉,微热,使其充分反应,生成NO的物质的量
| A.0.1mol | B.0.03mol | C.0.02mol | D.0.04mol |
下列实验现象与氧化还原反应有关的是
| A.蘸有浓盐酸和浓氨水的玻璃棒互相靠近,产生大量白烟 |
| B.向硅酸钠溶液中滴加适量的稀盐酸,有透明的凝胶形成 |
| C.将装有NO2 的试管倒立于水中,管内气体由红棕色逐渐转变为无色 |
| D.硫酸铁溶液中滴加硫氰化钾溶液变红 |
已知NH4CuSO3与足量的2 mol/L硫酸溶液混合微热,产生下列现象:①有红色金属生成;②产生刺激性气味的气体;③溶液呈现蓝色。据此判断下列说法正确的是
| A.反应中硫酸做氧化剂 |
| B.NH4CuSO3中硫元素被氧化 |
| C.1 mol NH4CuSO3完全反应转移0.5 mol电子 |
| D.刺激性气味的气体是氨气 |
已知常温下可用Co2O3制备Cl2,反应前后存在六种微粒:Co2O3、H2O、Cl2、H+、Cl-和Co2+。下列叙述不正确的是 ( )。
| A.氧化产物为Cl2 |
| B.参加反应的氧化剂与还原剂的物质的量之比为1∶2 |
| C.若有3 mol H2O生成,则反应中有2 mol电子转移 |
| D.当该反应生成2.24 L Cl2(标准状况)时,反应中有0.1 mol电子转移 |
a mol FeS与b mol FeO投入到V L、c mol/L的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看作是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为( )
①(a+b)×63 g ②(a+b)×189 g ③(a+b)mol ④[Vc-(9a+b)/3]mol
| A.①④ | B.②③ | C.①③ | D.②④ |
氯酸是一种强酸,浓度超过40%时会发生分解,该反应可表示为aHClO3―→bO2↑+cCl2↑+dHClO4+eH2O,下列有关说法不正确的是( )
| A.由反应可确定氧化性:HClO3>O2 |
| B.由非金属性:Cl>S,可推知酸性:HClO3>H2SO4 |
| C.若氯酸分解所得1 mol混合气体的质量为45 g,则反应方程式可表示为3HClO3=2O2↑+Cl2↑+HClO4+H2O |
| D.若化学计量数a=8,b=3,则生成3 mol O2时该反应转移20 mol电子 |
Na2FeO4是一种高效多功能水处理剂。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,下列说法中不正确的是( )
| A.Na2O2在上述反应中只作氧化剂 |
| B.Na2FeO4既是氧化产物又是还原产物 |
| C.Na2FeO4处理水时,既能杀菌,又能产生胶体净水 |
| D.2 mol FeSO4发生反应时,共有10 mol电子发生转移 |