题目内容
Li-SOCl2电池可用于心脏起搏器.该电池的电极材料分别为锂和碳,电解液是LiAlCl4—SOCl2.电池的总反应可表示为:4Li+2SOCl2 ==="4LiCl" +S +SO2.请回答下列问题:
(1)电池的负极材料为__________,发生的电极反应为__________________;
(2)电池正极发生的电极反应为_____________________________________;
(3)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成.如果把少量水滴到SOCl2中,反应的化学方程式为______________________________
(4)组装该电池必须在无水、无氧的条件下进行,原因是
.
(5)用此蓄电池电解含有0. 1 mol CuSO4和0. 1 mol NaCl的混合溶液100 mL,假如电路中转移了0.02 mol e-,且电解池的电极均为惰性电极,阳极产生的气体在标准状况下的体积是 L,将电解后的溶液加水稀释至1 L,此时溶液的pH= 。
(1)电池的负极材料为__________,发生的电极反应为__________________;
(2)电池正极发生的电极反应为_____________________________________;
(3)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成.如果把少量水滴到SOCl2中,反应的化学方程式为______________________________
(4)组装该电池必须在无水、无氧的条件下进行,原因是
.
(5)用此蓄电池电解含有0. 1 mol CuSO4和0. 1 mol NaCl的混合溶液100 mL,假如电路中转移了0.02 mol e-,且电解池的电极均为惰性电极,阳极产生的气体在标准状况下的体积是 L,将电解后的溶液加水稀释至1 L,此时溶液的pH= 。
(1)Li;4Li – 4 e- =" 4" Li+;
(2)2SOCl2+4 e- = 4Cl-+S+SO2↑;
(3)SOCl2+H2O = SO2↑+2HCl;
(4)SOCl2遇水易发生水解反应,其中S元素具有还原性,可被氧气氧化;
(5)0.224 ; 7
(2)2SOCl2+4 e- = 4Cl-+S+SO2↑;
(3)SOCl2+H2O = SO2↑+2HCl;
(4)SOCl2遇水易发生水解反应,其中S元素具有还原性,可被氧气氧化;
(5)0.224 ; 7
试题分析:结合电池总反应:4Li+2SOCl2 ="==4LiCl" +S +SO2 ,可知Li作负极,发生的电极反应为4Li – 4 e- =" 4" Li+;正极是碳,发生的电极反应是:2SOCl2+4 e- = 4Cl-+S+SO2↑。把少量水滴到SOCl2中,反应的化学方程式为SOCl2+H2O = SO2↑+2HCl。
由于SOCl2遇水易发生水解反应,且其中S元素具有还原性,可被氧气氧化,所以组装该电池必须在无水、无氧的条件下进行。
(5)用此蓄电池电解含有0. 1 mol CuSO4和0. 1 mol NaCl的混合溶液100 mL,假如电路中转移了0.02 mol e-,且电解池的电极均为惰性电极,阳极发生的反应是:2Cl— -2e-=Cl2↑,负极发生的阴极反应是:Cu2++2e-=Cu,阳极产生的气体在标准状况下的体积是
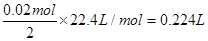 ,阴极有
,阴极有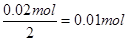 Cu析出,即Cu2+全部析出,则将电解后的溶液加水稀释至1 L,此时溶液为Na2SO4溶液,为中性溶液,pH为7。
Cu析出,即Cu2+全部析出,则将电解后的溶液加水稀释至1 L,此时溶液为Na2SO4溶液,为中性溶液,pH为7。点评:主要考查电解池原理知识及其计算题,此题为历年高考的常考题型,具有一定的难度,重在考查学生对电化学原理的掌握情况,以及培养学生分析问题,解决问题的能力。

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目