题目内容
【题目】实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,现取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4L.
请回答下列问题:
(1)写出该反应的离子反应方程式 .
(2)参加反应的二氧化锰的质量为 .
(3)反应中被氧化的HCl的物质的量为
【答案】
(1)MnO2+4H++2Cl﹣ ![]() Cl2↑+Mn2++2H2O
Cl2↑+Mn2++2H2O
(2)87g
(3)2mol
【解析】解:(1)反应的化学方程式为MnO2+4HCl(浓) ![]() MnCl2+C12↑+2H2O,改写为离子反应时二氧化锰、氯气、水在离子方程式中应保留化学式,则离子方程式为MnO2+4H++2Cl﹣
MnCl2+C12↑+2H2O,改写为离子反应时二氧化锰、氯气、水在离子方程式中应保留化学式,则离子方程式为MnO2+4H++2Cl﹣ ![]() Cl2↑+Mn2++2H2O,所以答案是:MnO2+4H++2Cl﹣
Cl2↑+Mn2++2H2O,所以答案是:MnO2+4H++2Cl﹣ ![]() Cl2↑+Mn2++2H2O;(2)氯气的物质的量为
Cl2↑+Mn2++2H2O;(2)氯气的物质的量为 ![]() =1mol,根据MnO2+4HCl(浓)
=1mol,根据MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,可知参加反应的二氧化锰物质的量为1mol,则参加反应二氧化锰的质量为1mol×87g/mol=87g,所以答案是:87g;(3)被氧化的HCl生成氯气,根据氯原子守恒,被氧化HCl的物质的量为1mol×2=2mol,
MnCl2+Cl2↑+2H2O,可知参加反应的二氧化锰物质的量为1mol,则参加反应二氧化锰的质量为1mol×87g/mol=87g,所以答案是:87g;(3)被氧化的HCl生成氯气,根据氯原子守恒,被氧化HCl的物质的量为1mol×2=2mol,
所以答案是:2mol.

【题目】合成氨对化学工业和国防工业具有重要意义。
(1)向合成塔中按物质的量之比l:4充入N2、H2进行氨的合成,图A为T℃时平衡混合物中氨气的体积分数与压强(p)的关系图。
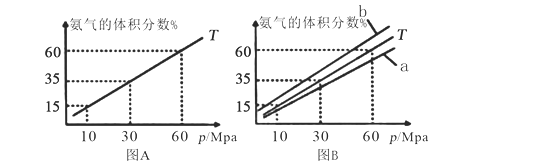
①图A中氨气的体积分数为15%时,H2的转化率为_______。
②图B中T=500℃,则温度为450℃时对应的曲线是_______(填“a”或“b”)。
(2)合成氨所需的氢气可由甲烷与水反应制得,反应的热化学方程式为:CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H>0,一定温度下,在体积为2 L的恒容容器中发生上述反应,各物质的物质的量变化如下表:
CO(g)+3H2(g) △H>0,一定温度下,在体积为2 L的恒容容器中发生上述反应,各物质的物质的量变化如下表:
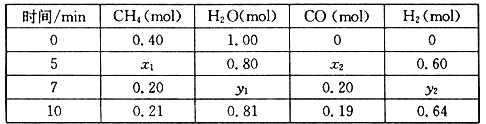
①分析表中数据,判断5 min时反应是否处于平衡状态?_____(填“是”或“否”)。
②该温度下,上述反应的平衡常数K=_____________________。
③反应在7~10 min内,CO的物质的量减少的原因可能是____________(填字母)。
a.减少CH4的物质的量 b.降低温度 c.升高温度 d.充入H2
④下列方法中可以证明上述反应已达平衡状态的是___________。
a.单位时间内生成3n mol H2的同时生成n mol CO
b.容器内压强不再变化
c.混合气体密度不再变化
d.混合气体的平均相对分子质量不再变化
e.CH4的质量分数不再变化
⑤已知碳的气化反应在不同温度下平衡常数的对数值(lgK)如下表:
气化反应式 | lgK | ||
700K | 900K | 1200K | |
C(s)+H2O(g)=CO(g)+H2(g) | -2.64 | -0.39 | 1.58 |
C(s)+2H2O(g)=CO2(g)+2H2(g) | -1.67 | -0.03 | 1.44 |
则反应CO(g)+H2O(g)![]() CO2(g)+H2(g)在900K时,该反应平衡常数的对数值(lgK)=_______。
CO2(g)+H2(g)在900K时,该反应平衡常数的对数值(lgK)=_______。
(3)在容积可变的密闭容器中发生反应:mA(g)+nB(g)![]() pC(g),在一定温度和不同压强下达到平衡时,分别得到A的物质的量浓度如下表:
pC(g),在一定温度和不同压强下达到平衡时,分别得到A的物质的量浓度如下表:
压强p/Pa | 2×105 | 5×105 | 1×106 |
c(A)/molL-1 | 0.08 | 0.20 | 0.44 |
①当压强从2×105Pa增加到5×105Pa时,平衡______移动(填“正向、逆向或不”)。
②当压强为1×106Pa时,此反应的平衡常数表达式为______________。