题目内容
25 ℃时,合成氨反应的热化学方程式为:
N2(g)+3H2(g) 2NH3(g)
△H=-92.4 kJ/mol
2NH3(g)
△H=-92.4 kJ/mol
在该温度时,取2mol N2和7 mol H2放在密闭容器中,在催化剂存在下进行反应,测得反应放出的热量总是[ ]
A.92.4 kJ B.92.4 kJ ~184.8 kJ
C.小于184.8 kJ D.184.8 kJ
【答案】
C
【解析】

练习册系列答案
 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
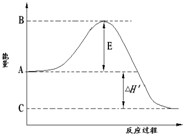 合成氨工业是极为重要的化学工业,当今对合成氨工业的研究仍然充满活力.其合成原理为:N2(g)+3H2(g)?2NH3(g);△H=-92.2kJ/mol.回答下列问题:
合成氨工业是极为重要的化学工业,当今对合成氨工业的研究仍然充满活力.其合成原理为:N2(g)+3H2(g)?2NH3(g);△H=-92.2kJ/mol.回答下列问题:
